Oxalsyre vs. Svovlsyretitrering:Hovedforskelle forklaret
Her er en opdeling:
Oxalsyre (H₂C₂O4)
* Diprotisk syre: Oxalsyre har to sure hydrogenatomer . Det betyder, at den kan donere to protoner (H⁺) pr. molekyle under titrering.
* Titreringskurve: Oxalsyrens titreringskurve vil vise to ækvivalenspunkter svarende til neutraliseringen af hvert surt brint. Det første ækvivalenspunkt vil være ved en lavere pH end det andet, da den anden proton lettere doneres.
Svovlsyre (H₂SO4)
* Stærk diprotisk syre: Svovlsyre er også en diprotisk syre , men det er en stærk syre . Dette betyder, at den første proton er fuldstændig dissocieret i opløsning, hvilket gør den til en stærk syre. Den anden proton er dog kun delvist dissocieret, hvilket gør den til en svagere syre.
* Titreringskurve: Titreringskurven for svovlsyre vil vise to ækvivalenspunkter , men det første ækvivalenspunkt vil være meget skarpere og forekomme ved en lavere pH end det andet. Dette skyldes, at den første proton er fuldstændig dissocieret og er en meget stærkere syre.
Nøgleforskelle under titrering:
* Antal ækvivalenspoint: Begge syrer har to ækvivalenspunkter på grund af deres diprotiske natur.
* Ækvivalenspunkt pH: Det første ækvivalenspunkt for svovlsyre vil være lavere end det første ækvivalenspunkt for oxalsyre på grund af svovlsyrens stærkere første proton.
* Skarphed af ækvivalenspunkter: Det første ækvivalenspunkt for svovlsyre vil være skarpere end det første ækvivalenspunkt for oxalsyre på grund af den første protons stærke sure natur.
Opsummering:
Mens både oxalsyre og svovlsyre er diprotiske syrer, adskiller deres titreringsadfærd sig på grund af de forskellige styrker af deres sure hydrogener. Oxalsyrens titreringskurve vil vise to distinkte ækvivalenspunkter, mens svovlsyrens kurve vil have et skarpere første ækvivalenspunkt på grund af dens første protons stærke sure natur.
 Varme artikler
Varme artikler
-
 Plantebaserede og genanvendelige plastikflasker med citrusskal som råmaterialeKredit:Pixabay/CC0 Public Domain Skiftet fra fossilbaseret til vedvarende bioplast kræver nye effektive metoder. Ny teknologi udviklet på VTT muliggør brugen af pektinholdigt landbrugsaffald, så
Plantebaserede og genanvendelige plastikflasker med citrusskal som råmaterialeKredit:Pixabay/CC0 Public Domain Skiftet fra fossilbaseret til vedvarende bioplast kræver nye effektive metoder. Ny teknologi udviklet på VTT muliggør brugen af pektinholdigt landbrugsaffald, så -
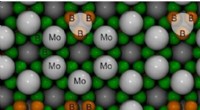 Forskere beregner krystalstruktur af superhårde molybdænboriderAtomarrangement i den højeste molybdænborid (MoB5-x) krystal Kredit:Dmitry V. Rybkovskiy, J. Phys. Chem. Lett. I deres søgen efter nye superhårde forbindelser, forskere har udført en forudsigelse
Forskere beregner krystalstruktur af superhårde molybdænboriderAtomarrangement i den højeste molybdænborid (MoB5-x) krystal Kredit:Dmitry V. Rybkovskiy, J. Phys. Chem. Lett. I deres søgen efter nye superhårde forbindelser, forskere har udført en forudsigelse -
 Undersøge vand af en elektrificerende årsagKAUST-forskere observerede, at vedhængende dråber dannet fra hydrofobe kapillærer til ensartede elektriske felter. Kredit:KAUST; Anastasia Serin Et eksperiment, elegant i sin enkelhed, hjælper med
Undersøge vand af en elektrificerende årsagKAUST-forskere observerede, at vedhængende dråber dannet fra hydrofobe kapillærer til ensartede elektriske felter. Kredit:KAUST; Anastasia Serin Et eksperiment, elegant i sin enkelhed, hjælper med -
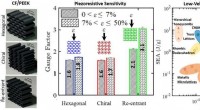 Letvægts, slagfaste bikagestrukturer kan fornemme, når de er blevet beskadigetGrafisk abstrakt. Kredit: Materialer og design (2021). DOI:10.1016/j.matdes.2021.109863 En ny form for letvægts, slagfaste plastbaserede honningkage-strukturer, der kan mærke, hvornår de er bleve
Letvægts, slagfaste bikagestrukturer kan fornemme, når de er blevet beskadigetGrafisk abstrakt. Kredit: Materialer og design (2021). DOI:10.1016/j.matdes.2021.109863 En ny form for letvægts, slagfaste plastbaserede honningkage-strukturer, der kan mærke, hvornår de er bleve
- Hvilken kraft er ansvarlig for at generere energien i vandmølle?
- Forskere laver ultrakompakt on-chip beregningsmæssigt infrarødt spektrometer
- Er der en rigtig måde at sige dit job op? Forskning viser, at nogle måder er bedre end andre
- En metode til selvovervåget robotlæring, der indebærer at sætte sig gennemførlige mål
- Atomer i SiO:Forståelse af siliciummonoxidsammensætning
- Jaws:Hvordan en afrikansk strålefinnet fisk hjælper os med at genoverveje evolutionens grundlægge…


