Syre-basetitrering:Eksempler og anvendelser - En omfattende vejledning
Eksempler på syre-basetitrering:
Syre-base titrering er en almindelig teknik, der bruges til at bestemme koncentrationen af en ukendt syre eller base opløsning. Her er nogle eksempler:
1. Bestemmelse af koncentrationen af eddike:
* Ukendt: Eddike (eddikesyreopløsning)
* Kendt: Natriumhydroxidopløsning (NaOH) med kendt koncentration
* Procedure: Et kendt volumen eddike titreres med standard NaOH-opløsningen ved hjælp af en pH-indikator (som phenolphtalein). Ækvivalenspunktet nås, når opløsningen bliver lyserød, hvilket indikerer, at al eddikesyre har reageret med NaOH.
* Beregning: Den anvendte mængde NaOH og dens koncentration bruges til at beregne koncentrationen af eddikesyre i eddike.
2. Bestemmelse af styrken af et antacidum:
* Ukendt: Antacida tablet indeholdende en base som calciumcarbonat (CaCO3)
* Kendt: Saltsyre (HCl) opløsning med kendt koncentration
* Procedure: En syreneutraliserende tablet opløses i et kendt volumen HCl. Den resulterende opløsning titreres derefter med en standard NaOH-opløsning. Mængden af NaOH anvendt til at neutralisere det overskydende HCl angiver mængden af syre neutraliseret af antacidet.
* Beregning: Mængden af syre neutraliseret af antacidet bruges til at bestemme antacidets "syreneutraliserende kapacitet".
3. Bestemmelse af koncentrationen af en svag syre:
* Ukendt: Svag syreopløsning som eddikesyre (CH3COOH)
* Kendt: Stærk baseopløsning som natriumhydroxid (NaOH) med kendt koncentration
* Procedure: Et kendt volumen af den svage syreopløsning titreres med standard NaOH-opløsningen under anvendelse af en pH-indikator. Ækvivalenspunktet nås, når opløsningen bliver lyserød.
* Beregning: Det anvendte volumen af NaOH og dets koncentration bruges til at beregne koncentrationen af den svage syre.
4. Bestemmelse af koncentrationen af en stærk base:
* Ukendt: Stærk baseopløsning som kaliumhydroxid (KOH)
* Kendt: Stærk syreopløsning som saltsyre (HCl) med kendt koncentration
* Procedure: Et kendt volumen af den stærke baseopløsning titreres med standard-HCl-opløsningen under anvendelse af en pH-indikator. Ækvivalenspunktet nås, når opløsningen bliver gul.
* Beregning: Det anvendte volumen af HCl og dets koncentration bruges til at beregne koncentrationen af den stærke base.
5. Måling af mængden af syre i vin:
* Ukendt: Vin (indeholder vinsyre)
* Kendt: Natriumhydroxidopløsning (NaOH) med kendt koncentration
* Procedure: Et kendt volumen vin titreres med standard NaOH-opløsningen ved hjælp af en pH-indikator. Ækvivalenspunktet nås, når opløsningen bliver lyserød.
* Beregning: Mængden af anvendt NaOH og dens koncentration bruges til at beregne mængden af vinsyre i vinen.
Dette er blot nogle få eksempler, men syre-basetitrering har mange anvendelser inden for forskellige områder som:
* Kemi: bestemmelse af koncentrationen af syrer og baser, verifikation af kemiske reaktioner og analyse af ukendte stoffer.
* Fødevarevidenskab: analysere surhedsgraden af fødevarer som eddike, vin og juice.
* Miljøvidenskab: analysere surhedsgraden af vandprøver.
* Medicin: måling af surhedsgraden af kropsvæsker som blod og urin.
At forstå principperne for syre-basetitrering og dens anvendelser er afgørende for en lang række videnskabelige og industrielle processer.
 Varme artikler
Varme artikler
-
 Visualisering af cementhydrering på et molekylært niveauKredit:CC0 Public Domain Betonverdenen, der omgiver os, skylder sin form og holdbarhed til kemiske reaktioner, der starter, når almindelig Portland -cement blandes med vand. Nu, MIT-forskere har d
Visualisering af cementhydrering på et molekylært niveauKredit:CC0 Public Domain Betonverdenen, der omgiver os, skylder sin form og holdbarhed til kemiske reaktioner, der starter, når almindelig Portland -cement blandes med vand. Nu, MIT-forskere har d -
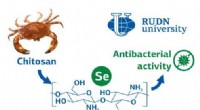 Kemikere syntetiserer en antimikrobiel forbindelse ud fra harmløst kitin og selenKredit:Russian Foundation for Basic Research RUDN-kemikere opnåede stoffer med høj antibakteriel aktivitet baseret på chitosan og selen. En af dem klarede sig endda bedre end almindelige antibiotik
Kemikere syntetiserer en antimikrobiel forbindelse ud fra harmløst kitin og selenKredit:Russian Foundation for Basic Research RUDN-kemikere opnåede stoffer med høj antibakteriel aktivitet baseret på chitosan og selen. En af dem klarede sig endda bedre end almindelige antibiotik -
 Forstå Forever Chemicals:Definition, Impact og SolutionsPramote Polyamate/Getty Images Levetiden for kemiske forbindelser varierer voldsomt; nogle nedbrydes hurtigt biologisk, hvilket gør dem til miljøvenlige materialer, men nogle ting vil ikke nedbrydes
Forstå Forever Chemicals:Definition, Impact og SolutionsPramote Polyamate/Getty Images Levetiden for kemiske forbindelser varierer voldsomt; nogle nedbrydes hurtigt biologisk, hvilket gør dem til miljøvenlige materialer, men nogle ting vil ikke nedbrydes -
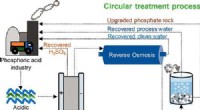 Forskere udvikler en metode til at omdanne farligt surt industrispildevand til værdifulde ressource…Kredit:ACS Sustainable Chemistry &Engineering (2022). DOI:10.1021/acssuschemeng.2c03132 Et forskerhold af miljøforskere fra Ben-Gurion University of the Negev har udviklet en cirkulær proces til at
Forskere udvikler en metode til at omdanne farligt surt industrispildevand til værdifulde ressource…Kredit:ACS Sustainable Chemistry &Engineering (2022). DOI:10.1021/acssuschemeng.2c03132 Et forskerhold af miljøforskere fra Ben-Gurion University of the Negev har udviklet en cirkulær proces til at
- Battle of the video-højttalere:Amazon Echo Show vs. Google Home Hub
- Nyt geoelektrisk farekort viser potentiel sårbarhed over for højspændingsnettet for to tredjedele…
- Hvem har rejst til månen, og hvornår?
- Et kig ind i hundens sind:ny undersøgelse afslører, hvordan hunde tænker på deres legetøj
- Hvilken videnskabsmand er ansvarlig for at se celler første gang?
- Fysikere skal skabe ny røntgendiagnostik til WEST-fusionsenheden i Frankrig


