Estimering af energien til at bryde obligationer i 2-buten:en trin-for-trin guide
1. Identificer obligationerne:
* 2-buten har en carbon-carbon-dobbeltbinding (C=C) og fem carbon-hydrogen-enkeltbindinger (C-H).
2. Beregn energien for dobbeltbindingen:
* Den gennemsnitlige bindingsentalpi for en C=C-binding er 614 kJ/mol.
3. Beregn energien for enkeltobligationer:
* Den gennemsnitlige bindingsentalpi for en CH-binding er 348 kJ/mol.
* Da der er 5 C-H-bindinger, er den samlede energi, der skal til for at bryde dem, 5 * 348 kJ/mol =1740 kJ/mol.
4. Samlet energi:
* For at bryde alle bindingerne i 2-buten skal du tilføje energien for dobbeltbindingen og enkeltbindingerne:614 kJ/mol + 1740 kJ/mol =2354 kJ/mol.
Derfor er den estimerede energi, der er nødvendig for at bryde alle bindingerne i 2-buten, 2354 kJ/mol.
Vigtig bemærkning: Dette er en estimeret værdi. Den faktiske nødvendige energi kan variere lidt afhængigt af det specifikke molekyle og dets miljø.
 Varme artikler
Varme artikler
-
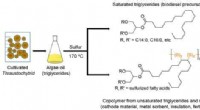 Simpel metode til at udvinde bioaktive stoffer af høj værdi fra encellet algeolieGrafisk abstrakt. Kredit:ACS Sustainable Chemistry &Engineering (2022). DOI:10.1021/acssuschemeng.1c08139 For at redde verdens fiskebestande og oceaner ræser forskere for at finde bedre og bæredygt
Simpel metode til at udvinde bioaktive stoffer af høj værdi fra encellet algeolieGrafisk abstrakt. Kredit:ACS Sustainable Chemistry &Engineering (2022). DOI:10.1021/acssuschemeng.1c08139 For at redde verdens fiskebestande og oceaner ræser forskere for at finde bedre og bæredygt -
 Observation af brinteffekter i metalDenne illustration viser hovedelementerne i det system, holdet brugte:Den flerfarvede plade i midten er det metallag, der studeres, det lyseblå område til venstre er elektrolytopløsningen, der bruges
Observation af brinteffekter i metalDenne illustration viser hovedelementerne i det system, holdet brugte:Den flerfarvede plade i midten er det metallag, der studeres, det lyseblå område til venstre er elektrolytopløsningen, der bruges -
 Ny forbindelse afslører grundlæggende egenskaber ved de mindste carbon nanorør1, 3-Diradicals indlejret i buede parafenylenenheder:Singlet versus triplet-tilstand. Virkningerne af krumningen bidrager til deres jordspintilstand. Kredit:Manabu Abe, Hiroshima Universitet Kemis
Ny forbindelse afslører grundlæggende egenskaber ved de mindste carbon nanorør1, 3-Diradicals indlejret i buede parafenylenenheder:Singlet versus triplet-tilstand. Virkningerne af krumningen bidrager til deres jordspintilstand. Kredit:Manabu Abe, Hiroshima Universitet Kemis -
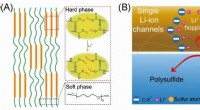 Stabiliserende svovlkatode med enkelt Li-ion-kanal polymerbindemiddel(A) Skematiske diagrammer over dannelsen af polymeren med enkeltionkanalerne. (B) Skematiske diagrammer af enkelt-ion-kanaler regulerer polysulfid- og Li-ion-hopningen. Kredit:©Science China Press
Stabiliserende svovlkatode med enkelt Li-ion-kanal polymerbindemiddel(A) Skematiske diagrammer over dannelsen af polymeren med enkeltionkanalerne. (B) Skematiske diagrammer af enkelt-ion-kanaler regulerer polysulfid- og Li-ion-hopningen. Kredit:©Science China Press
- Google viser ny telefon, enheder ved begivenheden i New York
- Er maling en forbindelse eller en blanding?
- Hvad er 12 fods pund svarende til i tomme pund?
- Højteknologisk, kugleformet arena, der kommer til Las Vegas Strip
- For ægte eller for falsk? Kvindelige Instagram influencers i 'ægthedsbinding'
- Enheden bringer silicium computerkraft til hjerneforskning og proteser


