BaCrO₄ + HCl Reaktion:Produkter og forklaring | Kemi forklaret
BaCrO4(s) + 2HCl(aq) → BaCl2(aq) + H₂CrO4(aq)
Her er en oversigt:
* BaCrO₄(s): Bariumkromat er en fast, gul forbindelse.
* HCl(aq): Saltsyre er en stærk syre i vandig opløsning.
* BaCl₂(vandig): Bariumchlorid er et opløseligt, farveløst salt.
* H2CrO4(vandig): Chromsyre er en svag syre.
Forklaring:
Reaktionen er en dobbelt forskydningsreaktion. Bariumet (Ba²⁺) fra bariumchromat kombineres med chloridionerne (Cl⁻) fra saltsyre og danner bariumchlorid (BaCl₂). Chromationerne (CrO₄²⁻) fra bariumchromat kombineres med hydrogenioner (H⁺) fra saltsyre og danner chromsyre (H₂CrO4).
Vigtige bemærkninger:
* Chromsyre er ustabil i opløsning og kan nedbrydes og danne dichromationer (Cr₂O₇²⁻) og vand (H₂O).
* Reaktionen udføres typisk i en fortyndet opløsning af saltsyre.
* Reaktionen er eksoterm, hvilket betyder, at den frigiver varme.
Sig til, hvis du har flere spørgsmål!
 Varme artikler
Varme artikler
-
 Hvorfor bomuld er det ultimative absorberende stofAf Kim Norton | Opdateret 24. marts 2022 Gargonia/iStock/GettyImages Når det kommer til badehåndklæder, er 100% bomuld fortsat guldstandarden for sugeevne. Bomuld kan suge op til 27 gange sin egen v
Hvorfor bomuld er det ultimative absorberende stofAf Kim Norton | Opdateret 24. marts 2022 Gargonia/iStock/GettyImages Når det kommer til badehåndklæder, er 100% bomuld fortsat guldstandarden for sugeevne. Bomuld kan suge op til 27 gange sin egen v -
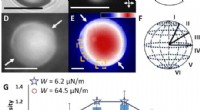 Programmering af van der Waals interaktioner med komplekse symmetrier til mikropartikler ved hjælp …Bipolære LC mikropartikler, eksperimenter, og teoretiske forudsigelser. Repræsentative (A) lysfelt- og (B) polariserede lysmikrofotografier (dobbelthovedede pile viser orienteringer af polarisatorer)
Programmering af van der Waals interaktioner med komplekse symmetrier til mikropartikler ved hjælp …Bipolære LC mikropartikler, eksperimenter, og teoretiske forudsigelser. Repræsentative (A) lysfelt- og (B) polariserede lysmikrofotografier (dobbelthovedede pile viser orienteringer af polarisatorer) -
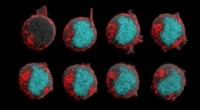 Forskere viser, at en kræftforsvarsmekanisme kan vendes tilbage for at angribe tumorerI disse time-lapse billeder, kimære antigenreceptorer reagerer på et opløseligt cytokin, udløser T-celleaktivering. Kredit:ZeNan Chang og Michael Lorenzini UCLA ingeniører og videnskabsmænd har ko
Forskere viser, at en kræftforsvarsmekanisme kan vendes tilbage for at angribe tumorerI disse time-lapse billeder, kimære antigenreceptorer reagerer på et opløseligt cytokin, udløser T-celleaktivering. Kredit:ZeNan Chang og Michael Lorenzini UCLA ingeniører og videnskabsmænd har ko -
 Forskere udvikler lovende ny type polymerLyse farver:SPPV -polymerer har mange vigtige teknologiske anvendelser. Kredit:TU Wien Organiske polymerer bruges i solceller, sensorer, LEDer og i mange andre enheder. En specifik type polymer, S
Forskere udvikler lovende ny type polymerLyse farver:SPPV -polymerer har mange vigtige teknologiske anvendelser. Kredit:TU Wien Organiske polymerer bruges i solceller, sensorer, LEDer og i mange andre enheder. En specifik type polymer, S
- Hvordan sukkerfrakke, der giver et middel til cellulær genkendelse, er kendt som?
- En blanding af gasformige kulbrinter placeret under overfladen Jorden ofte i nærheden af petroleu…
- Connecticut statslige agenturer målrettet i cyberangreb
- Hvordan ved vi at karamelliserende sukker er en kemisk forandring?
- Er puffere svage syrer eller baser, der kan reagere med stærke for at forhindre pludselige ændring…
- En instruktørvejledning til at reducere universitetsstuderendes stress og angst


