Arrhenius syrer og baser:definitioner og eksempler
Syrer:
* Producer hydrogenioner (H+), når de opløses i vand.
* Det betyder, at de øger koncentrationen af H+ ioner i opløsningen.
Baser:
* Producer hydroxidioner (OH-), når de opløses i vand.
* Det betyder, at de øger koncentrationen af OH-ioner i opløsningen.
Her er nogle eksempler:
Syrer:
* Saltsyre (HCl): HCl → H+ + Cl-
* Salpetersyre (HNO3): HNO3 → H+ + NO3-
* Svovlsyre (H2SO4): H2SO4 → 2H+ + SO42-
Baser:
* Natriumhydroxid (NaOH): NaOH → Na+ + OH-
* Kaliumhydroxid (KOH): KOH → K+ + OH-
* Calciumhydroxid (Ca(OH)2): Ca(OH)2 → Ca2+ + 2OH-
Nøglepunkter at huske om Arrhenius-teorien:
* Det fokuserer på opførsel af syrer og baser i vandige opløsninger.
* Det er en enkel og nyttig model til at forstå egenskaberne af syrer og baser, men den har begrænsninger.
* Det forklarer ikke adfærden af stoffer, der fungerer som syrer eller baser i ikke-vandige opløsningsmidler.
Sig til, hvis du gerne vil vide mere om andre syre-base teorier som Brønsted-Lowry eller Lewis!
Sidste artikelForståelse af nitrationladning:En detaljeret forklaring
Næste artikelEthan-strukturformel (C2H6) Forklaret - Kemihjælp
 Varme artikler
Varme artikler
-
 Oksekødspeptider blokerer for bitter smagKredit:American Chemical Society Fra burgere til bøffer, oksekød har en lang historie for at være en lækker del af aftensmaden. Men hvad nu hvis den behagelige oplevelse med at spise oksekød kunne
Oksekødspeptider blokerer for bitter smagKredit:American Chemical Society Fra burgere til bøffer, oksekød har en lang historie for at være en lækker del af aftensmaden. Men hvad nu hvis den behagelige oplevelse med at spise oksekød kunne -
 MRI-scanning hjælper med næste generations batteridesignKredit:CC0 Public Domain Magnetisk resonansbilleddannelse (MRI) kan give en effektiv måde at understøtte udviklingen af den næste generation af højtydende genopladelige batterier, ifølge forskni
MRI-scanning hjælper med næste generations batteridesignKredit:CC0 Public Domain Magnetisk resonansbilleddannelse (MRI) kan give en effektiv måde at understøtte udviklingen af den næste generation af højtydende genopladelige batterier, ifølge forskni -
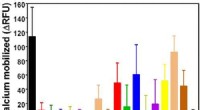
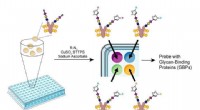 Ny TSRI-metode fremskynder undersøgelser af kulhydratbiologiEn ny metode til at samle et glycan-array. Kredit:Wu Lab / Scripps Research Institute 28. februar, 2018 - Næsten alle levende celler er besat med forgrenede kulhydratkæder kaldet glykaner. Glykane
Ny TSRI-metode fremskynder undersøgelser af kulhydratbiologiEn ny metode til at samle et glycan-array. Kredit:Wu Lab / Scripps Research Institute 28. februar, 2018 - Næsten alle levende celler er besat med forgrenede kulhydratkæder kaldet glykaner. Glykane -
 Tilsæt bare vand:Enkelt trin øger polymerers evne til at filtrere kuldioxid fra blandede gasserKredit:NC State Et internationalt team af forskere har fundet ud af, at det kan øge en eksisterende polymers evne til selektivt at fjerne kuldioxid (CO 2 ) ud af gasblandinger ved først at nedsæ
Tilsæt bare vand:Enkelt trin øger polymerers evne til at filtrere kuldioxid fra blandede gasserKredit:NC State Et internationalt team af forskere har fundet ud af, at det kan øge en eksisterende polymers evne til selektivt at fjerne kuldioxid (CO 2 ) ud af gasblandinger ved først at nedsæ
- Nogle kan ikke lide det varmt:Flaskehals for termisk ledningsevne-switching er løst
- Undersøgelse finder, at bykontorer pumper flygtige kemikalier ud til det fri, sammenlignet med traf…
- 20-årigt felteksperiment:Roter majs for bedre jordsundhed
- Hvad er teorien om, at jorden ydre skal ikke et stykke sten?
- Hvad hedder Astronut, der har tilbragt mest tid i rummet?
- En model af Mars-lignende protoplaneter kaster lys over tidlig solaktivitet


