Ny TSRI-metode fremskynder undersøgelser af kulhydratbiologi
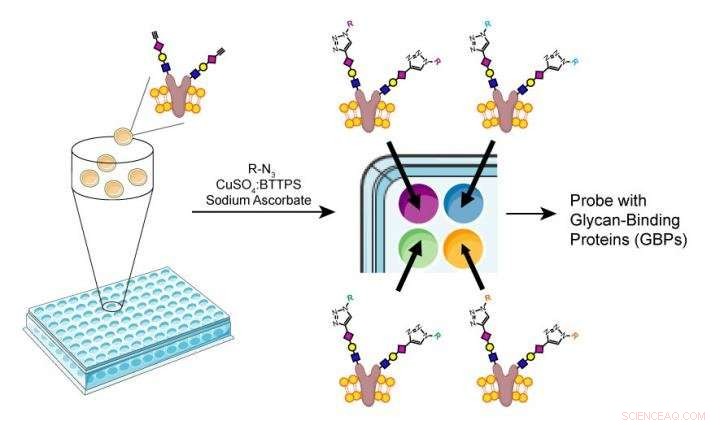
En ny metode til at samle et glycan-array. Kredit:Wu Lab / Scripps Research Institute
28. februar, 2018 - Næsten alle levende celler er besat med forgrenede kulhydratkæder kaldet glykaner. Glykaner spiller forskellige roller i at forme, hvordan en celle interagerer med sit miljø.
Nu, forskere ved The Scripps Research Institute (TSRI) har beskrevet en ny metode til at udsmykke celler med forskellige glykaner og screene interaktioner mellem glykaner og proteiner. Deres gennembrud, udgivet i dag i Naturkommunikation , kan udvide forskningen i glykaners rolle i menneskelige sygdomme, herunder kræftformer.
"Forskere har forsøgt at lave glycan-arrays, som enhver videnskabsmand, der er interesseret i glycaner, kan få adgang til i deres egne laboratorier i årevis, "siger Peng Wu, Ph.d., en TSRI-lektor og seniorforfatter af undersøgelsen. "Vi har ikke kun gjort det, men vi har gjort det på en måde, der er meget nem."
Forskere løser problemer med glykanscreening
Mønstrene af glycaner og glycan-bindende proteiner på en celles membran kan differentiere kræftceller fra raske celler, kontrollerer cellernes rolle i udviklingen og bidrager til forskellige interaktioner mellem voksne celler. Genetiske sygdomme, der påvirker cellernes evne til korrekt at skabe glykaner, kan forkorte levetiden og føre til muskuloskeletale problemer.
Men at studere glykaner har været notorisk vanskeligt. Mens forskere ved, hvordan man syntetiserer forskellige proteiner og DNA-molekyler i laboratoriet, at skabe glykaner efter behov har været kemisk udfordrende.
At studere hvilke proteiner i en celle, der interagerer med glycanmolekyler, forskere har typisk henvendt sig til glycan-bindingsarrays, hvor snesevis eller hundredvis af glykaner er fastgjort til et objektglas. Forskere udsætter derefter objektglasset for celler eller proteiner af interesse og observerer, om cellerne eller proteinerne klæber til glykanerne på objektglasset. Men at lave disse arrays er tidskrævende og dyrt.
"I fortiden, hvis du ville lave et array med 100 sukkerarter, så skulle du kemisk syntetisere 100 sukkerarter individuelt, hvilket kan være svært, " siger Wu. "Kun specialiserede kulhydratkemikere kan fremstille dem i visse laboratorier."
Wu og hans kolleger besluttede i stedet at udnytte kraften i de enzymer, som celler naturligt bruger til at producere glykaner. Disse enzymer arbejder trinvist for at skabe forgreningsglykaner - et lille stykke sukker fremstilles af et specialiseret enzym, så skaber et andet enzym den næste gren i kæden, og så videre. Forskerne fandt ud af, at selv strukturelt relaterede unaturlige sukkerarter kan tilføjes på denne måde.
Wus hold begyndte med muterede gnaverovarieceller, der havde et meget snævert repertoire af glykaner på deres overflade. Dette var et enklere system end at bruge menneskelige celler med mange typer glycaner. Forskerne udsatte derefter cellerne for forskellige sæt af glykandannende enzymer for at kontrollere tilsætningen af kulhydratgrene til glykanerne på hver celle.
Med denne metode, de skabte cellearrays hver besat med forskellige glykaner, inklusive unaturlige.
"Den eneste begrænsning er de enzymer, vi har til rådighed, og det faktum, at du skal starte med celler, der allerede har simpel glykosylering, "siger Wu." Men vi var i stand til at skabe alle de glycaner, vi ønskede. "
At sætte biblioteket på prøve
For at teste nytten af det nye cellematrix, Wu og hans kolleger screenede en række celler, hver viser forskellige glykaner, at bestemme, hvilke der er bundet til Siglec-15, et kendt glycan-bindende protein, der spiller en rolle i knogleudvikling og ombygning. Siglec-15 betragtes som et potentielt mål for lægemidler til behandling af postmenopausal osteoporose, så forståelse for, hvordan det interagerer med kulhydrater, er kritisk. Teamet identificerede tre strukturer med stærk binding til Siglec-15.
Forskerne inkuberede derefter humane osteoprogenitorceller med muterede gnaverovarieceller, der viste en af de tre strukturer under differentiering. Holdet fandt ud af, at denne proces undertrykte dannelsen af osteoklaster, en Siglec-15-udtrykkende knoglecelle, der absorberer knoglevæv under vækst og heling. Dette fund forstærker ideen om, at Siglec-15 er et godt mål for osteoporosebehandlinger, og at den nye glycan-screeningsstrategi kan pege forskere på lovende nye lægemidler.
"Vi ved ikke, om dette vil blive brugt i det brede samfund - det afhænger af tilgængeligheden af enzymer og celler, "siger Wu." Men hvis en hel flok celler med enkle og homogene glykaner kan stilles til rådighed, det ville være enormt for feltet."
 Varme artikler
Varme artikler
-
 Bioplast i bæredygtighedsdilemmaetTil dyrkning af sukkerrør, naturlig vegetation omdannes ofte til landbrugsjord og skove fældes. Kredit:OLOURBOX.de Plast fremstillet af afgrøder som majs eller sukkerrør i stedet for fossile brænd
Bioplast i bæredygtighedsdilemmaetTil dyrkning af sukkerrør, naturlig vegetation omdannes ofte til landbrugsjord og skove fældes. Kredit:OLOURBOX.de Plast fremstillet af afgrøder som majs eller sukkerrør i stedet for fossile brænd -
 Forskere udvikler en ny tilgang til at forudsige, hvordan væsker fryserKredit:Pixabay/CC0 Public Domain Forskere fra Queen Mary University of London har udviklet en ny beregningsmetode til bedre at forstå frysning i forskellige typer væsker. Processen med at fryse,
Forskere udvikler en ny tilgang til at forudsige, hvordan væsker fryserKredit:Pixabay/CC0 Public Domain Forskere fra Queen Mary University of London har udviklet en ny beregningsmetode til bedre at forstå frysning i forskellige typer væsker. Processen med at fryse, -
 At gøre polyurethan nedbrydeligt giver dets komponenter et nyt livDet nedbrydelige polyurethanmateriale (lyserød strimmel) kvælder og opløses derefter i syre blandet med et organisk opløsningsmiddel (venstre hætteglas på begge billeder), men ikke når det placeres i
At gøre polyurethan nedbrydeligt giver dets komponenter et nyt livDet nedbrydelige polyurethanmateriale (lyserød strimmel) kvælder og opløses derefter i syre blandet med et organisk opløsningsmiddel (venstre hætteglas på begge billeder), men ikke når det placeres i -
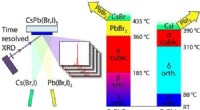 Højtydende solceller:Fysikere dyrker stabile perovskitlagKredit:ACS Krystallinske perovskitceller er nøglen til banebrydende tyndfilmsolceller. Selvom de allerede opnår meget høje effektivitetsniveauer i laboratoriet, kommercielle anvendelser er hæmmet
Højtydende solceller:Fysikere dyrker stabile perovskitlagKredit:ACS Krystallinske perovskitceller er nøglen til banebrydende tyndfilmsolceller. Selvom de allerede opnår meget høje effektivitetsniveauer i laboratoriet, kommercielle anvendelser er hæmmet
- Nye værktøjer hjælper lokalsamfund med at måle og reducere deres emissioner lokalt
- Big data på den sociale medieplatform afslører positive ansigtsudtryk af kvindelige besøgende i b…
- Kina undviger skylden for Qualcomm-NXP-fusionens død
- Nyopdagede bygninger afslører spor til gamle egyptiske dynastier
- Ny indsigt i, hvordan hund og mand jagede side om side, for over 8.000 år siden
- Dynamik af polymerkæder oven på forskellige materialer


