Ammoniak- og vandreaktion:Kemisk ligning og forklaring
NH3(aq) + H2O(l) ⇌ NH4+(aq) + OH⁻(aq)
Her er en oversigt:
* NH3(vandig) repræsenterer ammoniak opløst i vand (vandig opløsning).
* H2O(l) repræsenterer flydende vand.
* NH4+(vandig) repræsenterer ammoniumionen, dannet når ammoniak accepterer en proton (H⁺) fra vand.
* OH⁻(vandig) repræsenterer hydroxidionen, der dannes, når vand mister en proton.
Forklaring:
Ammoniak er en svag base, hvilket betyder, at den kan acceptere protoner. I nærværelse af vand vil en lille del af ammoniakmolekyler reagere med vandmolekyler, acceptere en proton og danne ammoniumioner (NH4⁺). Samtidig vil vandmolekyler miste en proton og danne hydroxidioner (OH⁻). Denne proces skaber en basisk opløsning på grund af tilstedeværelsen af hydroxidioner.
Nøglepunkter:
* Reaktionen er reversibel, hvilket betyder, at den kan fortsætte i begge retninger.
* Ligevægtspositionen favoriserer reaktanterne (ammoniak og vand) mere end produkterne (ammonium- og hydroxidioner). Det betyder, at de fleste ammoniakmolekyler forbliver uomsatte.
* Reaktionen er eksoterm, hvilket betyder, at den frigiver varme.
* Denne reaktion er vigtig for at forstå egenskaberne af ammoniak som base og dens evne til at neutralisere syrer.
 Varme artikler
Varme artikler
-
 Oprettelse af komplekse molekyler i nogle få trinLukas Gooßen og Stefania Trita arbejder på procedurer, der skal gøre produktionen af kemiske stoffer billigere og mere miljøvenlig. Kredit:RUB, Marquard. Dette billede må kun bruges til rapportering
Oprettelse af komplekse molekyler i nogle få trinLukas Gooßen og Stefania Trita arbejder på procedurer, der skal gøre produktionen af kemiske stoffer billigere og mere miljøvenlig. Kredit:RUB, Marquard. Dette billede må kun bruges til rapportering -
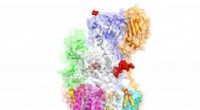 Cryo-EM afslører kritisk protein-modificerende kompleks og potentielt lægemiddelmålForskere har afsløret strukturen på atomniveau af et molekylært kompleks, der er ansvarligt for at modificere proteiner, muligvis baner vejen for udvikling af ny medicin mod kræft og en lang række and
Cryo-EM afslører kritisk protein-modificerende kompleks og potentielt lægemiddelmålForskere har afsløret strukturen på atomniveau af et molekylært kompleks, der er ansvarligt for at modificere proteiner, muligvis baner vejen for udvikling af ny medicin mod kræft og en lang række and -
 Dybdeafhængig valensstratificering i en lithium-rig lagdelt katodeen strukturel karakterisering af LirNMC katodemateriale ved XRD og Rietveld forfining. Den indsatte graf viser SEM-billedet af LirNMC-partikler. b Ladning-afladningsprofil og elektrokemiske cyklusdata
Dybdeafhængig valensstratificering i en lithium-rig lagdelt katodeen strukturel karakterisering af LirNMC katodemateriale ved XRD og Rietveld forfining. Den indsatte graf viser SEM-billedet af LirNMC-partikler. b Ladning-afladningsprofil og elektrokemiske cyklusdata -
 Ny behandling åbner mulighed for bagning af hindbærKøbte frosne hindbær (venstre) bevarer ikke deres form eller deres saft sammenlignet med behandlede hindbær (højre). Kredit:WSU Hindbærmuffins er i vores fremtid. Forskere fra Washington State Un
Ny behandling åbner mulighed for bagning af hindbærKøbte frosne hindbær (venstre) bevarer ikke deres form eller deres saft sammenlignet med behandlede hindbær (højre). Kredit:WSU Hindbærmuffins er i vores fremtid. Forskere fra Washington State Un
- Hvad er forskellen mellem farmaceutisk industri og kemisk industri?
- Kan smartphones besvare dit opkald om hjælp?
- Hvad er der bag en nr. 1-placering? Open-source LineUp-software muliggør granulær analyse af subje…
- Hvorfor sker bakterievækst?
- Hvilket instrument hjalp tidlige forskere med at opdage flere kroppe i solsystemet?
- Hvorfor har et bjerg mere energi end spabad?


