Berylliumfluoridbinding:Forståelse af den kovalente natur
Her er hvorfor:
* Elektronegativitet: Fluor er det mest elektronegative grundstof, mens beryllium har en relativt lav elektronegativitet. Denne store forskel i elektronegativitet betyder, at fluor tiltrækker de delte elektroner i bindingen meget stærkere end beryllium.
* Ionisk vs. kovalent: Mens elektronegativitetsforskellen er signifikant, er den ikke stor nok til at danne en rent ionbinding. De delte elektroner er tættere forbundet med fluor, men de deles stadig, hvilket resulterer i en polær kovalent binding.
Polær kovalent binding:
Det betyder, at bindingen har en delvis positiv ladning (δ+) på berylliumatomet og en delvis negativ ladning (δ-) på fluoratomet. Dette skaber et dipolmoment i BeF₂-molekylet.
Sidste artikelKemisk vs. kinetisk energi:Forstå de vigtigste forskelle
Næste artikelNatriumchlorid (NaCl):Forståelse af det kemiske forhold
 Varme artikler
Varme artikler
-
 At forstå, hvordan en katalysator omdanner metan til ethen, kan forhindre flaring af naturgasDeponi brænder flare af. Kredit:Eddie Hagler/Public Domain Det ville være en tredobbelt sejr - for klimaet, råmaterialeressourcer, og den kemiske industri. Med deres arbejde, videnskabsfolk ved Fr
At forstå, hvordan en katalysator omdanner metan til ethen, kan forhindre flaring af naturgasDeponi brænder flare af. Kredit:Eddie Hagler/Public Domain Det ville være en tredobbelt sejr - for klimaet, råmaterialeressourcer, og den kemiske industri. Med deres arbejde, videnskabsfolk ved Fr -
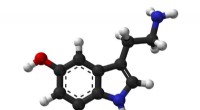 Forskerhold udvikler et nyt system til at spore hjernekemikalierBall-and-stick-model af serotonin-molekylet. Kredit:Public Domain Forskere ved UCLA og Columbia University har udviklet en ny metode til at spore aktiviteten af små molekyler i hjernen, herunder
Forskerhold udvikler et nyt system til at spore hjernekemikalierBall-and-stick-model af serotonin-molekylet. Kredit:Public Domain Forskere ved UCLA og Columbia University har udviklet en ny metode til at spore aktiviteten af små molekyler i hjernen, herunder -
 LSU Chemical Engineering afslører nye destillationskolonnerJohn Pendergast, professional-in-residence i Cain Department of Chemical Engineering, og John Flake, formand for Cain Department of Chemical Engineering. Kredit:LSU College of Engineering LSU Cain
LSU Chemical Engineering afslører nye destillationskolonnerJohn Pendergast, professional-in-residence i Cain Department of Chemical Engineering, og John Flake, formand for Cain Department of Chemical Engineering. Kredit:LSU College of Engineering LSU Cain -
 Forsker kortlægger kæmpe virusKristin Parent kortlagde strukturen af den gigantiske Samba-virus med MSUs kryo-EM-mikroskop, som er omtalt på forsiden af bladet Virus . Kredit:Michigan State University I et laboratorium v
Forsker kortlægger kæmpe virusKristin Parent kortlagde strukturen af den gigantiske Samba-virus med MSUs kryo-EM-mikroskop, som er omtalt på forsiden af bladet Virus . Kredit:Michigan State University I et laboratorium v
- Carbon nanorør udviklet til super effektiv afsaltning
- Nye administrerende direktører kan hæve deres sociale spil for at beholde deres job, siger undersø…
- Hvordan har rækkefølge en negativ effekt på et økosystem?
- Hvad er antallet af atomer i BO2?
- Forbedret 3-D nanoprintteknik til at bygge nanoskyskrabere
- Hvordan virker tyggegummi?


