Ædelgasser:Fælles egenskaber og karakteristika
* Fuld ydre skal af elektroner: Dette er det mest definerende træk ved ædelgasser. Deres yderste elektronskal er fuldstændig fyldt, hvilket giver dem en meget stabil elektronisk konfiguration. Dette gør dem utroligt ureaktive og svære at binde sammen med andre elementer.
* Farveløs, lugtfri og smagløs: I deres gasformige tilstand er de alle farveløse, lugtløse og smagløse. Dette skyldes deres manglende reaktivitet og deres simple atomstruktur.
* Dårlige ledere af varme og elektricitet: Deres mangel på frie elektroner bidrager til deres dårlige ledningsevne af varme og elektricitet.
* Lavt kogepunkt: Ædelgasser har meget lave kogepunkter, hvilket betyder, at de eksisterer som gasser ved stuetemperatur. Dette skyldes, at deres svage interatomiske kræfter gør det nemt for dem at gå over til den gasformige tilstand.
* Fundet i atmosfæren: Alle ædelgasser findes i atmosfæren, selvom nogle er til stede i spormængder.
Mens de deler disse vigtige ligheder, varierer de specifikke egenskaber for hver ædelgas, såsom massefylde og kogepunkt, afhængigt af deres atommasse og antallet af elektronskaller.
Opsummering: Ædelgasserne er en unik gruppe af grundstoffer med bemærkelsesværdigt ens egenskaber på grund af deres fulde ydre elektronskaller. Denne stabile konfiguration gør dem til de mindst reaktive elementer i det periodiske system.
Sidste artikelOxidationstal af CBr4:En trin-for-trin forklaring
Næste artikelForståelse af kovalente bindinger i vand (H₂O)
 Varme artikler
Varme artikler
-
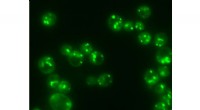 Et fedtregulerende enzym kunne holde nøglen til fedme, diabetes, Kræft, andre sygdommeFedt lagres i lipiddråber (lyse grønne pletter) i gærceller, hvilket er analogt med hvordan fedt lagres i menneskeligt væv. Kredit:Gil-Soo Han/Rutgers University-New Brunswick Det havde allerede v
Et fedtregulerende enzym kunne holde nøglen til fedme, diabetes, Kræft, andre sygdommeFedt lagres i lipiddråber (lyse grønne pletter) i gærceller, hvilket er analogt med hvordan fedt lagres i menneskeligt væv. Kredit:Gil-Soo Han/Rutgers University-New Brunswick Det havde allerede v -
 Mikroskala termoforese til at karakterisere hits fra high-throughput screeningMikroskala termoforese til at karakterisere hits fra high-throughput screening:et europæisk blyfabriksperspektiv. Kredit:European Lead Factory En ny perspektivartikel i marts 2018-udgaven af SLAS
Mikroskala termoforese til at karakterisere hits fra high-throughput screeningMikroskala termoforese til at karakterisere hits fra high-throughput screening:et europæisk blyfabriksperspektiv. Kredit:European Lead Factory En ny perspektivartikel i marts 2018-udgaven af SLAS -
 Fiksering af pulverkatalysatorer på elektroderDen nye metode udviklet af Corina Andronescu (i midten) og Stefan Barwe (til venstre for hende) sammen med deres kolleger, er potentielt interessant for den elektrokemiske brintproduktion. Kredit:RUB,
Fiksering af pulverkatalysatorer på elektroderDen nye metode udviklet af Corina Andronescu (i midten) og Stefan Barwe (til venstre for hende) sammen med deres kolleger, er potentielt interessant for den elektrokemiske brintproduktion. Kredit:RUB, -
 Når menneske og maskine er enige om iridiumoxidKredit:CC0 Public Domain Et menneskeligt forskerhold og en maskinlæringsalgoritme har fundet ud af, at vi er nødt til at genoverveje meget af det, vi ved om iridiumoxid. Iridiumoxid er en fremrag
Når menneske og maskine er enige om iridiumoxidKredit:CC0 Public Domain Et menneskeligt forskerhold og en maskinlæringsalgoritme har fundet ud af, at vi er nødt til at genoverveje meget af det, vi ved om iridiumoxid. Iridiumoxid er en fremrag
- Hvad er den geografiske placering af os, der bruger udtryk halvkugle og kontinent?
- Lavtemperaturkrystallisation af faserent α-formamidinium blyiodid muliggjort ved undersøgelse
- Hvilken energiprodukter ved vækkeur?
- Det seneste:Analytiker kalder Apple TV Plus prisshowstopper
- Hvad er sande udsagn om både nitrogen og ilt?
- Hvilken type energi bruges, når du klæder sig?


