Aluminium-svovlbinding:Forståelse af den ioniske binding
* Elektronegativitet: Aluminium (Al) har en elektronegativitet på 1,61, mens svovl (S) har en elektronegativitet på 2,58. Forskellen i elektronegativitet mellem disse to elementer er signifikant (2,58 - 1,61 =0,97), hvilket indikerer en stor forskel i deres evne til at tiltrække elektroner.
* Elektronoverførsel: Aluminium, et metal, har en tendens til at miste elektroner for at opnå en stabil oktetkonfiguration. Svovl, et ikke-metal, har en tendens til at få elektroner for at opnå en stabil oktetkonfiguration. I dette tilfælde vil aluminium miste tre elektroner for at danne en 3+ kation (Al³⁺), mens svovl vil få to elektroner til at danne en 2-anion (S²⁻).
* Ionisk bindingsdannelse: Den elektrostatiske tiltrækning mellem den positivt ladede aluminiumion (Al³⁺) og den negativt ladede svovlion (S²⁻) danner en ionbinding.
Derfor er den resulterende forbindelse aluminiumsulfid (Al₂S₃) , hvor forholdet mellem aluminium og svovlatomer er 2:3 for at opretholde elektrisk neutralitet.
Sidste artikelFermentering:Forståelse af pyruvatnedbrydning til ethanol og laktat
Næste artikelNatrium og svovl:Forståelse af ionisk binding
 Varme artikler
Varme artikler
-
 Opdagelse af en ny kilde til verdens dødeligste toksinForudsagt proteinstruktur af nyt botulinumneurotoksin eBonT/J. Billede:Quadram Institute Forskere fra Quadram Institute har identificeret gener, der koder for en tidligere uopdaget version af botu
Opdagelse af en ny kilde til verdens dødeligste toksinForudsagt proteinstruktur af nyt botulinumneurotoksin eBonT/J. Billede:Quadram Institute Forskere fra Quadram Institute har identificeret gener, der koder for en tidligere uopdaget version af botu -
 Nyt materiale kan opfange giftige forurenende stoffer fra luftenProfessor Michael Zaworotko, Bernal formand for Crystal Engineering and Science Foundation of Ireland Research Professor ved University of Limericks Bernal Institute. Nedenfor Dr. Xiang-Jing Kong fra
Nyt materiale kan opfange giftige forurenende stoffer fra luftenProfessor Michael Zaworotko, Bernal formand for Crystal Engineering and Science Foundation of Ireland Research Professor ved University of Limericks Bernal Institute. Nedenfor Dr. Xiang-Jing Kong fra -
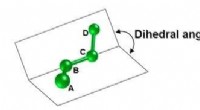 Fujitsu udvikler molekylær simuleringsteknologi til effektivt at skabe nye lægemiddelkandidaterFigur 1:Dihedral vinkel (vinklen dannet af planet skabt af atomer A, B, og C, og flyet skabt af atomer B, C, og D). Kredit:Fujitsu Fujitsu Laboratories annoncerede i dag udviklingen af molekylær
Fujitsu udvikler molekylær simuleringsteknologi til effektivt at skabe nye lægemiddelkandidaterFigur 1:Dihedral vinkel (vinklen dannet af planet skabt af atomer A, B, og C, og flyet skabt af atomer B, C, og D). Kredit:Fujitsu Fujitsu Laboratories annoncerede i dag udviklingen af molekylær -
 Bæredygtighed og effektivitet:de nye tendenser, der driver plastindustrienPlastøkonomien skal blive cirkulær. Kredit:Fraunhofer UMSICHT Med en samlet arbejdsstyrke på næsten 300, 000 ansatte, plast er en af Tysklands største industrisektorer. Industrien har også en st
Bæredygtighed og effektivitet:de nye tendenser, der driver plastindustrienPlastøkonomien skal blive cirkulær. Kredit:Fraunhofer UMSICHT Med en samlet arbejdsstyrke på næsten 300, 000 ansatte, plast er en af Tysklands største industrisektorer. Industrien har også en st
- Hvilken kraft er der mellem SO2 -molekyle?
- NASA ser dannelsen af Eastern Pacific Tropical Depression 16E
- Når to organismer lever i direkte fysisk kontakt med en, der muliggør i det mindste, kaldes organi…
- Hvordan kan jeg med sikkerhed observere en formørkelse uden at beskadige mine øjne, og er det sand…
- Forskere rækker tilbage gennem århundreders dyrkning for at spore, hvordan majs tilpassede forskel…
- Kvantesammenfiltring er det mærkeligste fænomen i fysik, men hvad er det?


