Ioniske vs. molekylære forbindelser:nøgleforskelle og egenskaber
Ioniske vs. molekylære forbindelser:En sammenligning
Her er en oversigt over de vigtigste forskelle mellem ioniske og molekylære forbindelser:
1. Limning:
* Ioniske forbindelser: Dannet gennem elektrostatisk tiltrækning mellem modsat ladede ioner. Disse ioner dannes ved fuldstændig overførsel af elektroner fra et metal til et ikke-metal.
* Molekylære forbindelser: Dannet ved deling af elektroner mellem ikke-metalatomer. Denne deling skaber kovalente bindinger.
2. Struktur:
* Ioniske forbindelser: Dann krystallinske strukturer med gentagne, tredimensionelle arrays af ioner.
* Molekylære forbindelser: Ofte eksisterer som diskrete molekyler med specifikke geometrier bestemt af arrangementet af atomer og deres delte elektroner.
3. Fysiske egenskaber:
| Ejendom | Ioniske forbindelser | Molekylære forbindelser |
|----------------|----------------|------------------------|
| Tilstand ved stuetemperatur | Typisk faste stoffer | Kan være faste stoffer, væsker eller gasser |
| Smeltepunkt | Høje smeltepunkter | Lavere smeltepunkter |
| Kogepunkt | Høje kogepunkter | Lavere kogepunkt |
| Opløselighed | Ofte opløseligt i vand | Kan være opløseligt eller uopløseligt i vand |
| Elektrisk ledningsevne | Gode ledere i smeltet tilstand eller opløst i vand | Dårlige konduktører |
4. Eksempler:
* Ioniske forbindelser: NaCl (bordsalt), CaCO3 (calciumcarbonat), MgO (magnesiumoxid)
* Molekylære forbindelser: H2O (vand), CO2 (kuldioxid), CH4 (methan)
5. Oversigt over nøgleforskelle:
| Funktion | Ioniske forbindelser | Molekylære forbindelser |
|----------------|----------------|------------------------|
| Bindning | Elektrostatisk tiltrækning (ioniske bindinger) | Kovalente bindinger |
| Struktur | Krystallinsk gitter | Diskrete molekyler |
| Fysiske egenskaber | Højt smelte-/kogepunkt, ofte opløseligt i vand, god elektrisk ledningsevne (i smeltet tilstand eller opløsning) | Lavere smelte-/kogepunkter, varierende opløselighed i vand, dårlig elektrisk ledningsevne |
Vigtig bemærkning: Nogle forbindelser kan udvise karakteristika for både ionisk og molekylær binding, hvilket gør dem vanskelige at kategorisere endeligt. Disse omtales ofte som "polære kovalente" forbindelser.
At forstå forskellene mellem ioniske og molekylære forbindelser er afgørende for at forstå deres egenskaber, reaktioner og anvendelser inden for forskellige områder som kemi, biologi og materialevidenskab.
 Varme artikler
Varme artikler
-
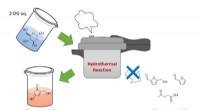 Forskere optimerer metoder til at producere nyttige forbindelser fra biomasseHydrotermisk reaktion under milde forhold. Kredit:Takaaki Kamishima Forskere har identificeret en et-trins proces til omdannelse af et plantebaseret sukker til en kemisk forbindelse, der kan bruge
Forskere optimerer metoder til at producere nyttige forbindelser fra biomasseHydrotermisk reaktion under milde forhold. Kredit:Takaaki Kamishima Forskere har identificeret en et-trins proces til omdannelse af et plantebaseret sukker til en kemisk forbindelse, der kan bruge -
 Forskere producerer de første open source-all-atom-modeller af COVID-19 spike proteinEn model af et S-protein. Kredit:Dr. Yeolkyo Choi/Lehigh Virus SARS coronavirus 2 (SARS-CoV-2) er den kendte årsag til coronavirus sygdom 2019 (COVID-19). Spike- eller S-proteinet letter viral ind
Forskere producerer de første open source-all-atom-modeller af COVID-19 spike proteinEn model af et S-protein. Kredit:Dr. Yeolkyo Choi/Lehigh Virus SARS coronavirus 2 (SARS-CoV-2) er den kendte årsag til coronavirus sygdom 2019 (COVID-19). Spike- eller S-proteinet letter viral ind -
 Forskere bruger lys til at kontrollere højhastighedskemiske reaktioner på en ny mådePolariserede optiske mikroskopibilleder af molekylerne ved 20 grader (A) og 51 grader Celsius (B). Kredit:Kato et al Mange naturlige og syntetiske kemiske systemer reagerer og ændrer deres egenska
Forskere bruger lys til at kontrollere højhastighedskemiske reaktioner på en ny mådePolariserede optiske mikroskopibilleder af molekylerne ved 20 grader (A) og 51 grader Celsius (B). Kredit:Kato et al Mange naturlige og syntetiske kemiske systemer reagerer og ændrer deres egenska -
 Teknik til at skabe medicin fri for bivirkningerJ. Julius Zhu sagde, at hovedideen bag forskningen var faktisk meget enkel, men det tog os mange år at få denne ting til at fungere. Kredit:Dan Addison, Universitetets kommunikation En ny teknik
Teknik til at skabe medicin fri for bivirkningerJ. Julius Zhu sagde, at hovedideen bag forskningen var faktisk meget enkel, men det tog os mange år at få denne ting til at fungere. Kredit:Dan Addison, Universitetets kommunikation En ny teknik
- Hvad er videnskaben om forhold til ting og rum og rum?
- Små kapsler, der forvandler sig på et øjeblik, kan være nøglen til at udvikle mindre elektronik…
- Rom tester genbrugsflasker til transitkontanter
- Hvilket stof var nødvendigt for at tilslutte sig insulingenbakterielt DNA?
- Kraftmasse ganget med acceleration ..... Hvor meget kraft er nødvendig for at fremskynde en 1000 kg…
- Hvordan bevares elektricitet?


