Beregning af HCl-masse for fuldstændig reaktion med ammoniak:en trin-for-trin guide
1. Afbalanceret kemisk ligning:
Den afbalancerede kemiske ligning for reaktionen mellem ammoniak og saltsyre er:
NH3(g) + HCl(g) → NH4Cl(s)
2. Molære masser:
* Molær masse af NH3 =14,01 g/mol + 3 (1,01 g/mol) =17,03 g/mol
* Molær masse af HCl =1,01 g/mol + 35,45 g/mol =36,46 g/mol
3. Støkiometri:
Den afbalancerede ligning viser et 1:1 molforhold mellem NH3 og HCl. Det betyder, at for hver 1 mol NH₃ skal du bruge 1 mol HCl for at reagere fuldstændigt.
4. Beregn mol ammoniak:
* Mol af NH₃ =(masse af NH₃) / (molær masse af NH₃)
* Mol NH3 =0,20 g / 17,03 g/mol =0,0117 mol
5. Beregn mol HCl:
* Da molforholdet er 1:1, mol HCl =mol NH3 =0,0117 mol
6. Beregn massen af HCl:
* Masse af HCl =(mol HCl) * (molær masse af HCl)
* Masse af HCl =0,0117 mol * 36,46 g/mol =0,43 g
Derfor skal du bruge ca. 0,43 gram HCl for at reagere fuldstændigt med 0,20 gram ammoniakgas.
Sidste artikelAmfoter HSO₄⁻:Forståelse af dets syre-base-adfærd
Næste artikelPhenol- og kaliumpermanganatreaktion:Mekanisme og produkter
 Varme artikler
Varme artikler
-
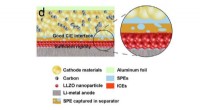 Forskere designer dendritfrit lithiumbatteriEn tynd asymmetrisk fast elektrolyt opfylder både kravene til litiummetal (blokering af dendritdannelse) og katode (muliggør lav grænseflademodstand). Kredit:H. Duan et al. ©2017 American Chemical Soc
Forskere designer dendritfrit lithiumbatteriEn tynd asymmetrisk fast elektrolyt opfylder både kravene til litiummetal (blokering af dendritdannelse) og katode (muliggør lav grænseflademodstand). Kredit:H. Duan et al. ©2017 American Chemical Soc -
 Computermodel kan hjælpe forskere med at skille sig op, gensamle proteiner på kommandoKredit:CC0 Public Domain At skilles og finde sammen igen er altid svært at gøre, men for proteiner, det er næsten umuligt. Imidlertid, en computerstyret algoritme kan hjælpe videnskabsmænd med at
Computermodel kan hjælpe forskere med at skille sig op, gensamle proteiner på kommandoKredit:CC0 Public Domain At skilles og finde sammen igen er altid svært at gøre, men for proteiner, det er næsten umuligt. Imidlertid, en computerstyret algoritme kan hjælpe videnskabsmænd med at -
 Forskere sætter et nyt spin på molekylær oxygen(a-c) AFM-billeder før (a) og efter (b) KPFS-manipulation af O annonce 2− −O annonce 2− med spidsen placeret symmetrisk i midten og de tilsvarende linjeprofiler (c). Det dobbelte lyspunkt blev
Forskere sætter et nyt spin på molekylær oxygen(a-c) AFM-billeder før (a) og efter (b) KPFS-manipulation af O annonce 2− −O annonce 2− med spidsen placeret symmetrisk i midten og de tilsvarende linjeprofiler (c). Det dobbelte lyspunkt blev -
 En metode til computerstøttet modellering og simulering af store proteiner og andre biomolekylerKredit:CC0 Public Domain To computerforskere ved Freie Universität Berlin ændrer måden, store proteiner modelleres inde i computere ved at kombinere maskinlæring, et område med kunstig intelligens
En metode til computerstøttet modellering og simulering af store proteiner og andre biomolekylerKredit:CC0 Public Domain To computerforskere ved Freie Universität Berlin ændrer måden, store proteiner modelleres inde i computere ved at kombinere maskinlæring, et område med kunstig intelligens
- Pinterest for at dirigere vaccinerelaterede søgninger til sundhedsorganisationer
- Sådan skaber du et synligt åndedræt:Videnskaben bag vanddampkondensering
- Sådan opsættes et Pareto-diagram i Minitab
- Brændstofmangel, flaskehalse hæmmer Floridas masseudvandring
- Maksimalt antal elektroner i det fjerde energiniveau?
- En maskine designet til at registrere hjernebølgemønstre produceret af elektrisk aktivitet af over…


