Amfoter HSO₄⁻:Forståelse af dets syre-base-adfærd
Her er en opdeling:
Som en syre:
* HSO₄⁻ kan donere en proton (H⁺) for at danne SO₄²⁻ (sulfation):
HSO4⁻ ⇌ H⁺ + SO₄²⁻
Som base:
* HSO₄⁻ kan acceptere en proton (H⁺) for at danne H₂SO4 (svovlsyre):
HSO4- + H+ ⇌ H2SO4
Denne dobbelte adfærd skyldes tilstedeværelsen af hydrogenatomet bundet til svovlatomet i HSO4-. Denne brint kan enten frigives som en proton (sur adfærd) eller kan tilsættes for at danne en anden binding (grundlæggende adfærd).
Opsummering:
HSO4⁻ er en amfiprotisk art, hvilket betyder, at den kan fungere som både en syre og en base afhængigt af reaktionsmiljøet.
 Varme artikler
Varme artikler
-
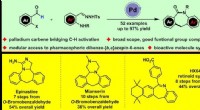 Modulær tilgang til dibenzo-fusionerede ε-lactamer gennem carbene-brodannende CH-aktiveringPalladiumkatalyseret adgang til dibenzo-fusionerede ε-lactamer og applikationen. Kredit:Prof. HUANGs gruppe På grund af deres spændende biologiske aktiviteter og potentielle anvendelighed til at t
Modulær tilgang til dibenzo-fusionerede ε-lactamer gennem carbene-brodannende CH-aktiveringPalladiumkatalyseret adgang til dibenzo-fusionerede ε-lactamer og applikationen. Kredit:Prof. HUANGs gruppe På grund af deres spændende biologiske aktiviteter og potentielle anvendelighed til at t -
 Forskere forbereder nyt lavtsmeltende, nitrogenholdigt, stannochlorophosphatglasSn-P-O-Cl-N glas fremstillet ved forskellige temperaturer. Kredit:SIOM Forskere fra Shanghai Institute of Optics and Fine Mechanics (SIOM) fra det kinesiske videnskabsakademi (CAS) har forberedt et
Forskere forbereder nyt lavtsmeltende, nitrogenholdigt, stannochlorophosphatglasSn-P-O-Cl-N glas fremstillet ved forskellige temperaturer. Kredit:SIOM Forskere fra Shanghai Institute of Optics and Fine Mechanics (SIOM) fra det kinesiske videnskabsakademi (CAS) har forberedt et -
 Variabel valens:Hvordan elementer ændrer deres ladningstilstande i kemiAf David Stewart • Opdateret 24. marts 2022 Elektroner kredser om en atomkerne i diskrete energiniveauer. De yderste elektroner - kendt som valenselektroner - bestemmer, hvordan et atom interagerer m
Variabel valens:Hvordan elementer ændrer deres ladningstilstande i kemiAf David Stewart • Opdateret 24. marts 2022 Elektroner kredser om en atomkerne i diskrete energiniveauer. De yderste elektroner - kendt som valenselektroner - bestemmer, hvordan et atom interagerer m -
 Kemikere udvikler sikre alternativer til phthalater, der bruges i plastRebecca Braslaus laboratorium har arbejdet på at udvikle ikke-migrerende blødgøringsmidler, der ikke kan udvaskes af plastik og forurene fødevarer og miljøet. Kredit:Carolyn Lagattuta Forskere ved
Kemikere udvikler sikre alternativer til phthalater, der bruges i plastRebecca Braslaus laboratorium har arbejdet på at udvikle ikke-migrerende blødgøringsmidler, der ikke kan udvaskes af plastik og forurene fødevarer og miljøet. Kredit:Carolyn Lagattuta Forskere ved
- Hvor mange protoner neutroner og elektroner har et menneske?
- Franske brandmænd kæmper mod Riviera-inferno for tredje dag
- Hvad er et spormineral?
- Smash and grab:En sværvægtsstjernemester for døende stjerner
- Hvad er den kemiske sammensætning af vismut?
- Hvis en kasse er stationær på en hældning, betyder det, at i ligevægtstilstanden?


