Variabel valens:Hvordan elementer ændrer deres ladningstilstande i kemi
Af David Stewart • Opdateret 24. marts 2022
Elektroner kredser om en atomkerne i diskrete energiniveauer. De yderste elektroner - kendt som valenselektroner - bestemmer, hvordan et atom interagerer med andre. Atomer stræber efter at nå en stabil konfiguration svarende til den nærmeste ædelgas, typisk ved at donere, acceptere eller dele disse elektroner. Denne adfærd omtales som et atoms valens.
TL;DR
Variabel valens beskriver et elements evne til at udvise forskellige ladningstilstande afhængigt af reaktionen. For eksempel danner jern FeO med en +2 valens og Fe2O3 med en +3 valens.
Valens og binding
Når et atom donerer eller accepterer valenselektroner, skaber det ofte en ionbinding. Omvendt, når atomer deler disse elektroner, dannes en kovalent binding. Begge typer bindinger er centrale for kemiske forbindelsers struktur og egenskaber.
Variabel Valency
Nogle elementer klæber ikke til en enkelt valens. Deres oxidationstilstande varierer med det kemiske miljø, hvilket påvirker egenskaberne af de resulterende forbindelser. Jerns skift fra +2 i ferrooxid (FeO) til +3 i ferrioxid (Fe2O3) eksemplificerer dette fænomen. Den magnetiske opførsel af disse oxider adskiller sig tilsvarende.
Elementer, der udviser variabel valens
- Overgangsmetaller:jern (Fe), nikkel (Ni), kobber (Cu), tin (Sn)
- Ikke-metaller:nitrogen (N), oxygen (O), brint (H)
Eksempler omfatter hydrogenperoxid (H2O2), hvor brint har en +2 valens, versus vand (H2O), hvor hydrogen er +1. Nitrogen forekommer i ammonium (NH4+), hvor det har en -3 valens, og i lattergas (N2O), hvor det er +1.
Repræsenterer variabel valens
Kemikere angiver et grundstofs oxidationstilstand med et romertal i hævet ved siden af dets symbol. For eksempel P V Cl5 angiver, at fosfor er i tilstanden +5 i fosforpentachlorid.
Data hentet fra International Union of Pure and Applied Chemistry (IUPAC) og standardlærebøger om uorganisk kemi.
 Varme artikler
Varme artikler
-
 Sådan adskilles ilt fra flydende luft på en sikker måde:en trin-for-trin guideAf David Hoskins • Opdateret 24. marts 2022 Brugen af flydende ilt er steget på tværs af forskellige sektorer - fødevarekonservering, medicinsk terapi og rumfart. Flydende luft opnås ved at afkøle at
Sådan adskilles ilt fra flydende luft på en sikker måde:en trin-for-trin guideAf David Hoskins • Opdateret 24. marts 2022 Brugen af flydende ilt er steget på tværs af forskellige sektorer - fødevarekonservering, medicinsk terapi og rumfart. Flydende luft opnås ved at afkøle at -
 Forskerteam viser komplekse, 3D-printede schwarzitter modstår tryk, når de er belagtEn komprimeringstest af 3D-printede schwarzitter, der enten er belagt eller ikke-belagt med en tynd polymer, viser, hvordan polymeren holder keramikken i stykker. Materialerne kan bruges hvor som hels
Forskerteam viser komplekse, 3D-printede schwarzitter modstår tryk, når de er belagtEn komprimeringstest af 3D-printede schwarzitter, der enten er belagt eller ikke-belagt med en tynd polymer, viser, hvordan polymeren holder keramikken i stykker. Materialerne kan bruges hvor som hels -
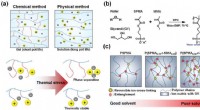 Et termometer, der kan strækkes og deformeres af vandVirkningerne af ionisk sidekæde. a) Skema, der angiver forskel med hensyn til brugstid og termisk stabilitet i henhold til kemiske og fysiske metoder. b) Skema for P(SPMA-r-MMA)er og vandopløselighed.
Et termometer, der kan strækkes og deformeres af vandVirkningerne af ionisk sidekæde. a) Skema, der angiver forskel med hensyn til brugstid og termisk stabilitet i henhold til kemiske og fysiske metoder. b) Skema for P(SPMA-r-MMA)er og vandopløselighed. -
 Processen til at tilpasse molekyler virker dobbeltRice University kandidatstuderende Kang-Jie (Harry) Bian opstiller lysfølsomme molekyler til et eksperiment i laboratoriet hos kemiker Julian West. Bian er hovedforfatter af en undersøgelse inspireret
Processen til at tilpasse molekyler virker dobbeltRice University kandidatstuderende Kang-Jie (Harry) Bian opstiller lysfølsomme molekyler til et eksperiment i laboratoriet hos kemiker Julian West. Bian er hovedforfatter af en undersøgelse inspireret
- Hvilken proces repræsenterer en kemisk ændring ... smeltning af is eller fordampningsvand?
- Hvad er gravitationsacceleration?
- Hvilket udtryk repræsenterer størrelsen af hastighedsvektoren?
- Reflekterer stjerner lys fra solen?
- NASA observerer orkanen Sally, der lander tidligt om morgenen i Alabama
- Nye fund - Indbrudstyve har en af fire personligheder, og de bliver endelig fanget


