Processen til at tilpasse molekyler virker dobbelt

Rice University kandidatstuderende Kang-Jie (Harry) Bian opstiller lysfølsomme molekyler til et eksperiment i laboratoriet hos kemiker Julian West. Bian er hovedforfatter af en undersøgelse inspireret af naturlige processer for at muliggøre modulær difunktionalisering af alkenmolekyler til design af lægemidler og materialer. Kredit:Rice University
Inspireret af din lever og aktiveret af lys viser en kemisk proces udviklet i laboratorier på Rice University og i Kina løfter for lægemiddeldesign og udvikling af unikke materialer.
Forskere ledet af riskemikeren Julian West og Xi-Sheng Wang ved University of Science and Technology of China, Hefei, rapporterer om deres vellykkede katalytiske proces til samtidig at tilføje to distinkte funktionelle grupper til enkelte alkener, organiske molekyler hentet fra petrokemikalier, der indeholder mindst en carbon-carbon dobbeltbinding kombineret med hydrogenatomer.
Endnu bedre, siger de, er, at disse alkener er "uaktiverede" - det vil sige, de mangler reaktive atomer i nærheden af dobbeltbindingen - og indtil nu har de vist sig at være udfordrende at forstærke.
Den kemiske vej beskrevet i Journal of the American Chemical Society kunne forenkle oprettelsen af et bibliotek af prækursorer til den farmaceutiske industri og forbedre fremstillingen af polymerer.
West, hvis laboratorium designer syntetiske kemiske processer, sagde, at den første inspiration kom fra et enzym, cytochrom P450, leveren bruger til at eliminere potentielt skadelige molekyler.
"Disse enzymer er en slags buzzsaws, der maler molekyler, før de kan få dig i problemer," sagde han. "De gør dette gennem en interessant mekanisme kaldet radikal rebound."
West sagde, at P450 finder carbon-hydrogen-bindinger og fjerner brinten og efterlader et carbon-centreret radikal, der inkluderer en uparret elektron.
"Den elektron ønsker virkelig at finde en partner, så P450 vil straks give et iltatom tilbage ("rebound"), hvilket oxiderer molekylet," sagde han. "I kroppen hjælper det med at deaktivere disse molekyler, så du kan slippe af med dem.
"Denne form for rebound er kraftfuld," sagde West. "Og Harry (hovedforfatter Kang-Jie Bian, en ris-studerende) spekulerede på, om vi kunne gøre noget lignende for at overføre forskellige fragmenter til den radikale."
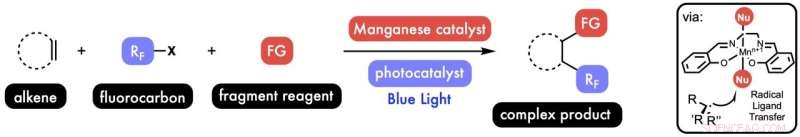
Rice University kemikere udviklede en metode til at tilføje to fragmenter til et alkenmolekyle i en enkelt proces. Opdagelsen kunne forenkle design af lægemidler og materialer. Kredit:West Research Group/Rice University
Deres løsning var at muliggøre, hvad de kalder radikal ligandoverførsel, en generel metode, der bruger mangan til at katalysere den "radikale rebound".
West sagde, mens P450 bruger det nærliggende element, jern, til at katalysere den biologiske reaktion, viste tidligere eksperimenter på Rice-laboratoriet og andre steder, at mangan havde potentiale.
"Mangan hjalp processen med at være mere selektiv og en lille smule mere aktiv, såvel som meget billigere og nemmere," forklarede han. "Det kan overføre en masse forskellige atomer - som klor, nitrogen og svovl - bare ved at ændre, hvilken kommerciel ingrediens du tilføjer til reaktionen."
Den reaktion tegnede sig for én funktionalisering. Hvorfor ikke gå efter to?
West sagde, at Bian også kom med ideen om at tilføje en fotokatalysator til blandingen. "Når du skinner lys på det, bliver det ophidset, og du kan gøre ting, der ville være umulige i grundtilstanden, som at aktivere små fluorcarbonmolekyler for at lave radikale fragmenter, der har kulstof-fluorbindinger, som er vigtige for farmaceutisk og materialevidenskab, " han sagde. "Nu kan vi knytte disse til vores molekyle af interesse."
Slutresultatet er en mild og modulær proces til at tilføje to funktionelle grupper til en enkelt alken i ét trin.
"Først har vi carbon-carbon dobbeltbindingen af et molekyle af interesse, alkenen," sagde West og opsummerede. "Så tilføjer vi dette værdifulde fluorcarbon, og så svømmer mangankatalysatoren op og overfører denne radikale ligand for at tilføje et klor- eller nitrogen- eller svovlatom."
Han bemærkede, at samarbejdet mellem Rice og Wangs laboratorium var et naturligt resultat af Bians flytning til Rice fra Hefei, hvor han fik sin mastergrad. "Vi fokuserede virkelig på mangan-aspektet af dette arbejde, og Wangs gruppe bragte ikke kun ekspertise inden for fotokatalyse, men også udviklede og testede kulstof-fluor-fragmenter og viste, at de ville fungere rigtig godt i dette system," sagde West.
Han sagde, at sammen med farmaceutisk og materialevidenskab kunne kemisk biologi også drage fordel af processen, især for dens affinitet til pClick, en metode opdaget af riskemikeren Han Xiao til at binde lægemidler eller andre stoffer til antistoffer.
Medforfattere er Rice undergraduate David Nemoto Jr. og kandidatstuderende Shih-Chieh Kao, og Yan He og Yan Li fra Hefei. Wang er professor ved Hefei. West er Norman Hackerman-Welch Young Investigator og assisterende professor i kemi. + Udforsk yderligere
Har du travlt med at udvikle medicin? Her er din chat
Sidste artikelOrganopbevaring et skridt nærmere med kryokonservering
Næste artikelUpcycling af plast gennem dynamisk tværbinding
 Varme artikler
Varme artikler
-
 Kemikalier af høj værdi til lægemidler kan gøres billigere og grønnere af nye katalysatorerForskere fra venstre mod højre:Jonathan Barrios-Rivera, Martin Wills, Yingjian Xu. Kredit:University of Warwick Kemikalier af høj værdi, der bruges til at fremstille lægemidler, kunne gøres meget
Kemikalier af høj værdi til lægemidler kan gøres billigere og grønnere af nye katalysatorerForskere fra venstre mod højre:Jonathan Barrios-Rivera, Martin Wills, Yingjian Xu. Kredit:University of Warwick Kemikalier af høj værdi, der bruges til at fremstille lægemidler, kunne gøres meget -
 Proteiner som shuttle service til målrettet administration af medicinKredit:FAU/Johannes Schweininger Præcis målretning af medicin er ikke længere en vision for fremtiden. Friedrich-Alexander-Universität Erlangen-Nürnberg (FAU) har med succes udviklet proteiner, de
Proteiner som shuttle service til målrettet administration af medicinKredit:FAU/Johannes Schweininger Præcis målretning af medicin er ikke længere en vision for fremtiden. Friedrich-Alexander-Universität Erlangen-Nürnberg (FAU) har med succes udviklet proteiner, de -
 Ultrahurtig kompression tilbyder en ny måde at få makromolekyler ind i cellerneBilledet viser en mikrofluidisk chip, hvortil der er tilføjet farvestof for at vise kanalerne. Ved at behandle levende celler som små svampe, forskere har udviklet en potentielt ny måde at introducere
Ultrahurtig kompression tilbyder en ny måde at få makromolekyler ind i cellerneBilledet viser en mikrofluidisk chip, hvortil der er tilføjet farvestof for at vise kanalerne. Ved at behandle levende celler som små svampe, forskere har udviklet en potentielt ny måde at introducere -
 Avancerede biomaterialer med silkefibroin-bioaktivt glas til at konstruere patientspecifikke 3D-knog…Udvikling af avancerede hybride biomaterialer ved hjælp af tilpasset 3D-printsoftware. Kredit:RoboCAD, 3D blæk, LLC, doi:10.1088/1748-605X/aad2a9 Den komplekse arkitektur af knogler er udfordrende
Avancerede biomaterialer med silkefibroin-bioaktivt glas til at konstruere patientspecifikke 3D-knog…Udvikling af avancerede hybride biomaterialer ved hjælp af tilpasset 3D-printsoftware. Kredit:RoboCAD, 3D blæk, LLC, doi:10.1088/1748-605X/aad2a9 Den komplekse arkitektur af knogler er udfordrende
- Smart grids:Forbedrer modstandskraften
- Undersøgelse afslører overflod af mikroskopiske malingsflager i Nordatlanten
- Gør bleer til klistermærker:Brug kemisk genbrug til at forhindre millioner af tons affald
- Team afslører molekylær struktur af vand ved guldelektroder
- Billede:Pilanesberg, Sydafrika
- Metaloxider holder nøglen til billige, grøn energi


