Nedbrydning ved opvarmning:Hvilke forbindelser kan og ikke kan nedbrydes
* Kemisk stabilitet: Nogle forbindelser er i sagens natur meget stabile og kræver ekstreme temperaturer eller andre forhold for at bryde deres bindinger. For eksempel har mange ioniske forbindelser som natriumchlorid (NaCl) meget høje smelte- og kogepunkter, og opvarmning alene vil ikke nedbryde dem.
* Dekomponeringsprodukter: Selvom en forbindelse kan nedbrydes ved opvarmning, kan de resulterende produkter være endnu mere stabile. For eksempel nedbryder opvarmningsvand (H₂O) det til brint (H₂) og oxygen (O₂), som begge er stabile gasser.
* Reversibilitet for reaktion: Nogle nedbrydningsreaktioner er reversible. Opvarmning af en forbindelse kan få den til at nedbrydes, men afkøling kan få produkterne til at rekombinere. Et klassisk eksempel er nedbrydningen af calciumcarbonat (CaCO₃) til calciumoxid (CaO) og kuldioxid (CO₂). Afkøling af reaktionen vil få produkterne til at rekombinere.
Eksempler på forbindelser, der ikke let nedbrydes ved opvarmning:
* Ædelgasser: Disse elementer er allerede i deres mest stabile form og nedbrydes ikke let af varme.
* Mange ioniske forbindelser: Som tidligere nævnt har disse ofte meget høje smelte- og kogepunkter.
* Visse organiske molekyler: Nogle organiske molekyler er meget stabile og kræver særlige betingelser for nedbrydning.
Eksempler på forbindelser, der let nedbrydes ved opvarmning:
* Karbonater: Mange carbonater, som calciumcarbonat (CaCO₃), nedbrydes ved opvarmning for at frigive kuldioxidgas.
* Hydrater: Disse forbindelser indeholder vandmolekyler bundet til en metalion. Opvarmning kan drive vandmolekylerne væk.
* Visse organiske forbindelser: Mange organiske molekyler kan nedbrydes ved opvarmning, hvilket fører til dannelsen af nye forbindelser.
Opsummering: Selvom opvarmning kan være en måde at nedbryde nogle forbindelser på, er det ikke en universel metode. Nedbrydningen af en forbindelse afhænger af dens kemiske stabilitet, stabiliteten af dens potentielle nedbrydningsprodukter og reaktionens reversibilitet.
 Varme artikler
Varme artikler
-
 Vand danner rygsøjlen med hydrering omkring DNA, gruppe finderEn illustration af, hvad kiral ikke-lineær spektroskopi afslører:at DNA er omgivet af en chiral vand-superstruktur, danner en rygsøjle af hydrering. Kredit:Poul Petersen Vand er Jordens mest rigel
Vand danner rygsøjlen med hydrering omkring DNA, gruppe finderEn illustration af, hvad kiral ikke-lineær spektroskopi afslører:at DNA er omgivet af en chiral vand-superstruktur, danner en rygsøjle af hydrering. Kredit:Poul Petersen Vand er Jordens mest rigel -
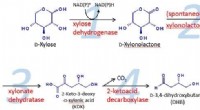 Metabolisk ingeniørmetode lykkes med at producere 1, 2, 4-butantetriol bæredygtigt fra biomasseFigur 1:Diagram over reaktionsprocessen. Kredit:Kobe University En mere miljøvenlig og bæredygtig metode til fremstilling af det nyttige kemikalie 1, 2, 4-butantetriol er blevet opdaget. Kobe -uni
Metabolisk ingeniørmetode lykkes med at producere 1, 2, 4-butantetriol bæredygtigt fra biomasseFigur 1:Diagram over reaktionsprocessen. Kredit:Kobe University En mere miljøvenlig og bæredygtig metode til fremstilling af det nyttige kemikalie 1, 2, 4-butantetriol er blevet opdaget. Kobe -uni -
 Biomolekyle metal-organiske hybrider med høj bioaktivitetKredit:Wiley Biomakromolekyler inkorporeret i skræddersyede metal-organiske rammer ved hjælp af peptidmodulatorer er godt afskærmede, men yderst aktive takket være omhyggeligt afstemt nanoarkitekt
Biomolekyle metal-organiske hybrider med høj bioaktivitetKredit:Wiley Biomakromolekyler inkorporeret i skræddersyede metal-organiske rammer ved hjælp af peptidmodulatorer er godt afskærmede, men yderst aktive takket være omhyggeligt afstemt nanoarkitekt -
 Udvikling af et bredt temperaturområde og højspændingsvandige MXene plane mikro-superkondensatore…(a) Det elektrokemiske stabilitetsvindue for højkoncentreret LiCl-vandig elektrolyt udvider sig til ~ 2,7 V. (b) Spændingsvinduet for MXene-elektrode i højkoncentreret LiCl-vandig elektrolyt udvides t
Udvikling af et bredt temperaturområde og højspændingsvandige MXene plane mikro-superkondensatore…(a) Det elektrokemiske stabilitetsvindue for højkoncentreret LiCl-vandig elektrolyt udvider sig til ~ 2,7 V. (b) Spændingsvinduet for MXene-elektrode i højkoncentreret LiCl-vandig elektrolyt udvides t
- Hvad er det grå goo mareridt?
- Hvad er betydningen af almindelige laboratorieapparater inden for videnskab?
- Relativistisk selvfokusering giver mid-IR-drevne elektroner et boost
- Har stoffer med høj termisk energi hurtigt bevægelige partikler?
- Sådan beregnes afstanden, hastigheden og tiden
- Hvilken forbindelse gør Tin Carbon og Oxygen?


