Oxidationsnummer:Forståelse af atomiske ladninger i forbindelser
Her er en oversigt:
* Ioniske forbindelser: I ioniske forbindelser er oxidationstallet simpelthen ladningen af ionen. For eksempel i NaCl er oxidationstallet for natrium (Na) +1 og oxidationstallet for chlor (Cl) er -1.
* Kovalente forbindelser: I kovalente forbindelser, hvor elektroner deles, tildeles oxidationstallet baseret på et sæt regler, der bestemmer den relative elektronegativitet af de involverede atomer.
* Regler for tildeling af oxidationsnumre:
* Oxidationstallet for et grundstof i dets grundstofform er altid 0.
* Summen af oxidationstallene i et neutralt molekyle er 0.
* Summen af oxidationstallene i en polyatomisk ion er lig med ladningen af ionen.
* Gruppe 1 metaller har altid et oxidationstal på +1.
* Gruppe 2 metaller har altid et oxidationstal på +2.
* Fluor har altid et oxidationstal på -1.
* Oxygen har normalt et oxidationstal på -2 (undtagen i peroxider, hvor det er -1, og i forbindelser med fluor, hvor det kan være positivt).
* Brint har normalt et oxidationstal på +1 (undtagen i metalhydrider, hvor det er -1).
* Brug af oxidationsnumre:
* Forudsigelse af kemiske reaktioner: Oxidationstal hjælper os med at identificere, hvilke atomer der bliver oxideret (taber elektroner), og hvilke der bliver reduceret (får elektroner) i en kemisk reaktion.
* Afbalancering af redoxreaktioner: Oxidationstal er afgørende for at afbalancere komplekse redoxreaktioner.
* Nomenklatur: Oxidationsnumre bruges nogle gange i navngivningen af forbindelser.
Vigtige punkter at huske:
* Oxidationstal er teoretiske værdier og repræsenterer ikke nødvendigvis de faktiske ladninger på atomerne.
* Oxidationstal kan være fraktioner.
* Nogle atomer kan have flere oxidationsnumre afhængigt af den forbindelse, de er i.
Forståelse af oxidationstal er afgørende for at mestre kemikoncepter som redoxreaktioner, afbalancering af kemiske ligninger og forståelse af strukturen og bindingen i molekyler.
 Varme artikler
Varme artikler
-
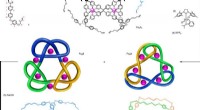 Forskere skaber det mest sammenfiltrede sammenlåste molekyle nogensindeDen 12 komponent (6 × ligand 1; 6 × Fe 2+ ) samling af det mellemliggende hexamere cirkulære helikat [Fe 6 1 6 ](PF 6 ) 12 og syntesen af +31#+31#+31 sammensatte knude 2 og 9 3 7 link
Forskere skaber det mest sammenfiltrede sammenlåste molekyle nogensindeDen 12 komponent (6 × ligand 1; 6 × Fe 2+ ) samling af det mellemliggende hexamere cirkulære helikat [Fe 6 1 6 ](PF 6 ) 12 og syntesen af +31#+31#+31 sammensatte knude 2 og 9 3 7 link -
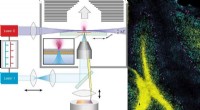 Innovativ metode giver unik indsigt i strukturen af celler og vævTil venstre:hvordan t-MALDI-2-MS billeddannelsesmetoden fungerer. Til højre:et eksempel, hvor den komplekse struktur af en mus cerebellum vises ved hjælp af overlejring af tre ionsignaler. Kredit:Natu
Innovativ metode giver unik indsigt i strukturen af celler og vævTil venstre:hvordan t-MALDI-2-MS billeddannelsesmetoden fungerer. Til højre:et eksempel, hvor den komplekse struktur af en mus cerebellum vises ved hjælp af overlejring af tre ionsignaler. Kredit:Natu -
 Krystalklar opløsningsmiddelfiltreringMembranen adskilte effektivt en blanding af to farvestoffer (blå) i dens komponenter, bliver ferskvandsgul. Kredit:The American Chemical Society Kovalente organiske materialer med velordnede porøs
Krystalklar opløsningsmiddelfiltreringMembranen adskilte effektivt en blanding af to farvestoffer (blå) i dens komponenter, bliver ferskvandsgul. Kredit:The American Chemical Society Kovalente organiske materialer med velordnede porøs -
 Katalysator fremstillet af jern kan drive en vigtig reaktion for fremstilling af organiske forbindel…Keio University-forskere har fundet en måde at erstatte det dyre ædelmetal ruthenium (billedet) med en simpel jernkatalysator til carbon-hydrogen-alkylering af aromatiske ketoner med alkener. Kredit:S
Katalysator fremstillet af jern kan drive en vigtig reaktion for fremstilling af organiske forbindel…Keio University-forskere har fundet en måde at erstatte det dyre ædelmetal ruthenium (billedet) med en simpel jernkatalysator til carbon-hydrogen-alkylering af aromatiske ketoner med alkener. Kredit:S
- 3D-trykt robothånd spiller klaver
- Hvilke typer energi får du, når du brænder brændstof?
- NASA annoncerer to missioner for at studere det tidlige solsystem
- NASA-satellitter opdager, hvad der driver nordlyset
- Hvorfor bruges 2 molekyler ATP til at starte processen anaerob respiration?
- En planet med mere end 16 måner?


