Natrium vs. Klor Atomstørrelse i NaCl:Forståelse af ionisk binding
* Ionisk binding: I NaCl mister natrium en elektron for at blive en positivt ladet natriumion (Na⁺), mens klor får en elektron til at blive en negativt ladet chloridion (Cl⁻). Denne overførsel af elektroner danner en ionbinding.
* Effektiv nuklear ladning: Når natrium mister sin yderste elektron, har det nu færre elektroner og det samme antal protoner (positive ladninger i kernen). Det betyder, at de resterende elektroner trækkes stærkere ind af kernen, hvilket resulterer i en mindre ionradius .
* Elektronafskærmning: Klor får på den anden side en elektron. Dette øgede antal elektroner øger elektron-elektron frastødning, hvilket gør elektronskyen større. Derudover går den ekstra elektron ind i et højere energiniveau, hvilket øger størrelsen yderligere.
Opsummering: Tabet af en elektron i natrium fører til en *stærkere* tiltrækning mellem de resterende elektroner og kernen, hvilket resulterer i en mindre ionradius. Forstærkningen af en elektron i klor fører til en *svagere* tiltrækning mellem elektronerne og kernen, hvilket resulterer i en større ionradius.
 Varme artikler
Varme artikler
-
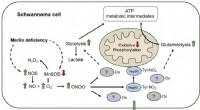 Forskere tager et vigtigt skridt mod kræftbehandlinger, der efterlader sunde celler uskadteForskere har åbnet en mulig vej til nye kræftbehandlinger, der ikke har de bivirkninger, der ofte ledsager mange nuværende kræftbehandlinger ved at identificere en proteinmodifikation, der specifikt u
Forskere tager et vigtigt skridt mod kræftbehandlinger, der efterlader sunde celler uskadteForskere har åbnet en mulig vej til nye kræftbehandlinger, der ikke har de bivirkninger, der ofte ledsager mange nuværende kræftbehandlinger ved at identificere en proteinmodifikation, der specifikt u -
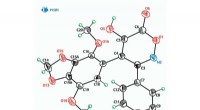 Kemikere forenkler syntesen af antitumorforbindelserKredit:RUDN Universitet En RUDN-kemiker i samarbejde med kolleger fra N.D. Zelinsky Institute of Organic Chemistry og N.K. Koltsov Institut for Udviklingsbiologi (IDB), RAS har udviklet en ny meto
Kemikere forenkler syntesen af antitumorforbindelserKredit:RUDN Universitet En RUDN-kemiker i samarbejde med kolleger fra N.D. Zelinsky Institute of Organic Chemistry og N.K. Koltsov Institut for Udviklingsbiologi (IDB), RAS har udviklet en ny meto -
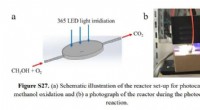 Effektivitet i fotokatalyse viste sig at være stedfølsomSupplerende billede af testapparatet. Kredit:https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.202014037 Prof. Huang Weixin og Zhang Qun fra University of Science and Technology of China (USTC)
Effektivitet i fotokatalyse viste sig at være stedfølsomSupplerende billede af testapparatet. Kredit:https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.202014037 Prof. Huang Weixin og Zhang Qun fra University of Science and Technology of China (USTC) -
 Ny metode hjælper med at kvantificere reversibilitet og irreversibilitet af praktiske Li-metalbatte…Metoden til afkobling og kvantificering af aktiv Li og død Li. Kredit:NIMTE En forskergruppe ledet af prof. Liu Zhaoping ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under d
Ny metode hjælper med at kvantificere reversibilitet og irreversibilitet af praktiske Li-metalbatte…Metoden til afkobling og kvantificering af aktiv Li og død Li. Kredit:NIMTE En forskergruppe ledet af prof. Liu Zhaoping ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under d
- Hvad består af solen?
- Forskere sikrer højopløsningsmålinger for CO2-diplomati
- Hvilken type mineral er den vigtigste komponent de fleste klipper på jorden?
- Japans SoftBank vil investere 900 millioner euro i Tysklands Wirecard
- Hvad er uraffineret olie?
- Hvordan tidevandet påvirker grundvandet under vores fødder


