Gruppe 1-metaller:Forståelse af deres høje reaktivitet
Her er hvorfor:
* Lav ioniseringsenergi: De mister let deres yderste elektron for at danne en +1 kation, hvilket gør dem til stærke reduktionsmidler.
* Stor atomstørrelse: Deres ydre elektron er længere væk fra kernen og svagt tiltrukket, hvilket gør det nemmere at fjerne.
* Svag metallisk binding: Den svage binding bidrager til deres blødhed og lave smelte- og kogepunkter.
Denne høje reaktivitet betyder, at de reagerer kraftigt med vand, ilt og andre ikke-metaller. For eksempel reagerer lithium, natrium og kalium eksplosivt med vand.
Vigtig bemærkning: På grund af deres høje reaktivitet opbevares gruppe 1 metaller typisk under olie for at forhindre reaktion med luft og fugt.
Sidste artikelHydrogen Ion vs. Proton:Forstå forskellen
Næste artikelLithiumsulfatdannelse:Neutralisering af svovlsyre med lithiumhydroxid
 Varme artikler
Varme artikler
-
 Biologisk materiale øger solcellens ydeevneCongcong Wu, forskningslektor ved Penn State, arbejder med materialer, der kan indsættes i næste generation af solceller for at forbedre deres effektivitet. Perovskite solceller er et område med inten
Biologisk materiale øger solcellens ydeevneCongcong Wu, forskningslektor ved Penn State, arbejder med materialer, der kan indsættes i næste generation af solceller for at forbedre deres effektivitet. Perovskite solceller er et område med inten -
 Undersøgelse afslører karakteristika ved SARS-CoV-2 spike proteinBillede af den ultrastrukturelle morfologi udstillet af 2019 Novel Coronavirus (2019-nCoV). Kredit:CDC En ny University of Kentucky College of Medicine undersøgelse offentliggjort i Journal of Bi
Undersøgelse afslører karakteristika ved SARS-CoV-2 spike proteinBillede af den ultrastrukturelle morfologi udstillet af 2019 Novel Coronavirus (2019-nCoV). Kredit:CDC En ny University of Kentucky College of Medicine undersøgelse offentliggjort i Journal of Bi -
 Ny metode til at løse plastiks bæredygtighedsproblemDr. Junpeng Wang. Kredit:University of Akron Bæredygtighed i plast er kommet langt i de seneste år, i høj grad takket være videnskabelige fremskridt. Men selvom plast bliver mere og mere miljøvenl
Ny metode til at løse plastiks bæredygtighedsproblemDr. Junpeng Wang. Kredit:University of Akron Bæredygtighed i plast er kommet langt i de seneste år, i høj grad takket være videnskabelige fremskridt. Men selvom plast bliver mere og mere miljøvenl -
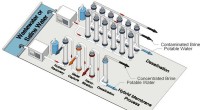 Membran kan bedre behandle spildevand, genvinde værdifulde ressourcerForskere foreslår, at nuværende afsaltningsprocesser og fremtidige hybride bruger en blokpolymermembran til at behandle ukonventionelle vandkilder. Kredit:University of Notre Dame billede/Yizhou Zhang
Membran kan bedre behandle spildevand, genvinde værdifulde ressourcerForskere foreslår, at nuværende afsaltningsprocesser og fremtidige hybride bruger en blokpolymermembran til at behandle ukonventionelle vandkilder. Kredit:University of Notre Dame billede/Yizhou Zhang
- Ny forskning viser, at bæredygtighed kan være et salgsargument for nye ingredienser
- Kan du observere faserne af Mars på jorden?
- Mængden af et materiale i et bestemt volumen et andet materiale?
- Hvilken industri bruger smeltning i stof?
- Hvad bruges til at måle et forslag?
- Hvad er hovedideen af forskellige slags økosystemer består af planter og dyr Hvorfor?


