Magnesiumhydrid (MgH2):Struktur, binding og krystalgitter
Her er hvorfor:
* Ionisk binding: Magnesium (Mg) er et metal og taber let to elektroner for at danne en +2-kation (Mg²⁺). Hydrogen (H) er et ikke-metal og optager let en elektron for at danne en -1 anion (H⁻). Den stærke elektrostatiske tiltrækning mellem disse modsat ladede ioner danner ionbindingen.
* Krystalgitter: I magnesiumhydrid arrangerer Mg²⁺- og H⁻-ionerne sig i en gentagen, tredimensionel struktur kaldet et krystalgitter. Denne struktur maksimerer tiltrækningskræfterne mellem ionerne, mens de frastødende kræfter minimeres.
Derfor er det forkert at tale om den "molekylære form" af magnesiumhydrid. I stedet beskriver vi krystalstrukturen af den ioniske forbindelse.
Sidste artikelHydrogenatomer i NaOH:En kemisk formelopdeling
Næste artikelHCN Molecule Shape:Forståelse af den lineære geometri
 Varme artikler
Varme artikler
-
 Gør plastik mere gennemsigtigt og tilføjer samtidig elektrisk ledningsevneJay Guo har et ark med fleksibel gennemsigtig dirigent på University of Michigans College of Engineering North Campus. Materialet lægger et tyndt lag sølv mellem to dielektriske materialer, aluminiumo
Gør plastik mere gennemsigtigt og tilføjer samtidig elektrisk ledningsevneJay Guo har et ark med fleksibel gennemsigtig dirigent på University of Michigans College of Engineering North Campus. Materialet lægger et tyndt lag sølv mellem to dielektriske materialer, aluminiumo -
 Forskere opfinder håndholdt enhed til hurtig overvågning af drikkevandskvalitetenNTU -forskere udviklede en bærbar enhed, inspireret af menneskekroppens evne, at opdage spor af tungmetaller i drikkevand på bare fem minutter. L-R:Assoc Prof Yong Ken-Tye og hans ph.d.-studerende Ste
Forskere opfinder håndholdt enhed til hurtig overvågning af drikkevandskvalitetenNTU -forskere udviklede en bærbar enhed, inspireret af menneskekroppens evne, at opdage spor af tungmetaller i drikkevand på bare fem minutter. L-R:Assoc Prof Yong Ken-Tye og hans ph.d.-studerende Ste -
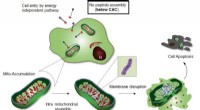 Forskere finder en ny måde at tackle kræftceller påFigur viser Intra-mitokondriel samling af Mito-FF. Kredit:UNIST Montering på stedet af amfifile peptider med ledsagende cellulære funktioner inde i en levende celle (dvs. intracellulær samling) og
Forskere finder en ny måde at tackle kræftceller påFigur viser Intra-mitokondriel samling af Mito-FF. Kredit:UNIST Montering på stedet af amfifile peptider med ledsagende cellulære funktioner inde i en levende celle (dvs. intracellulær samling) og -
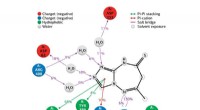 Chemist syntetiserer nye forbindelser med stærke antidiabetiske egenskaberKredit:RUDN Universitet En kemiker fra RUDN University har syntetiseret nye derivater af 1, 2, 4-triazol, der udviser antidiabetiske egenskaber. Eksperimenter viste, at disse forbindelser virker b
Chemist syntetiserer nye forbindelser med stærke antidiabetiske egenskaberKredit:RUDN Universitet En kemiker fra RUDN University har syntetiseret nye derivater af 1, 2, 4-triazol, der udviser antidiabetiske egenskaber. Eksperimenter viste, at disse forbindelser virker b
- Mister Flat Beer sit alkoholindhold?
- NASAs fjerntliggende rumopdagelse (Ultima Thule) ser ud som en snemand
- Hæve IQ af smarte vinduer
- En fortælling om to pulsarer:Plumes tilbyder geometriundervisning til astronomer
- Orkanen Dorian:Hvor den ramte, hvor er den på vej hen, og hvorfor så ødelæggende
- Forsker tilbyder øget forståelse af korrosion i kalkovne fyret med biobrændsel


