Heliumforbindelser:Udforskning af undtagelserne for inerthed
Her er en opdeling:
Hvorfor helium er ureaktivt:
* Ædelgaskonfiguration: Helium har en fuld ydre skal af elektroner (2 elektroner i sin 1s orbital). Dette gør det meget stabilt og modstandsdygtigt over for at få eller tabe elektroner for at danne kemiske bindinger.
* Høj ioniseringsenergi: Det kræver meget energi at fjerne en elektron fra et heliumatom, hvilket yderligere hindrer dets deltagelse i kemiske reaktioner.
* Svage interatomiske kræfter: Heliumatomer interagerer kun svagt med hinanden, primært gennem van der Waals-kræfter. Dette gør det til en gas selv ved meget lave temperaturer.
Kendte heliumforbindelser:
* Helium Excimers: Disse er kortlivede molekyler i exciteret tilstand, der dannes, når heliumatomer udsættes for højenergiforhold som elektriske udladninger eller laserexcitation. Eksempler inkluderer He2* og HeNe*.
* Heliumhydridion (HeH+): Dette er den eneste kendte stabile forbindelse af helium, der eksisterer under normale forhold. Det er dannet i det interstellare medium og er blevet observeret spektroskopisk.
* Heliumklynger: Ved ekstremt lave temperaturer kan heliumatomer svagt associere med hinanden og danne klynger. Det er dog ikke ægte kemiske forbindelser i traditionel forstand.
Samlet set:
Mens helium faktisk er ekstremt ureaktivt og danner meget få forbindelser, er det ikke helt nøjagtigt at sige, at der ikke eksisterer nogen forbindelser. Der er en håndfuld kendte undtagelser, herunder excimere, heliumhydridion og klynger. Langt størstedelen af helium forbliver dog ubundet på grund af dets unikke elektroniske konfiguration og høje stabilitet.
 Varme artikler
Varme artikler
-
 Forskere udvikler hurtigere test for hashkvalitetKredit:CC0 Public Domain Med den kommende legalisering af cannabis i Canada, producenter leder i stigende grad efter hurtige og præcise midler til at bestemme deres produkters styrke og kvalitet.
Forskere udvikler hurtigere test for hashkvalitetKredit:CC0 Public Domain Med den kommende legalisering af cannabis i Canada, producenter leder i stigende grad efter hurtige og præcise midler til at bestemme deres produkters styrke og kvalitet. -
 Bestemmelse af kemiske egenskaber:En praktisk vejledning til nøjagtig stofidentifikationsfe-co2/iStock/GettyImages Oversigt Identifikation af et stofs kemiske egenskaber er afgørende for sikkerhed, overholdelse og effektiv anvendelse. Ved at udføre systematiske eksperimenter, der udsætt
Bestemmelse af kemiske egenskaber:En praktisk vejledning til nøjagtig stofidentifikationsfe-co2/iStock/GettyImages Oversigt Identifikation af et stofs kemiske egenskaber er afgørende for sikkerhed, overholdelse og effektiv anvendelse. Ved at udføre systematiske eksperimenter, der udsætt -
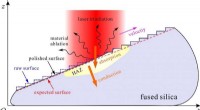 CO2 -laserablation fører en ny vej til skræddersyede kontinuerlige smeltede silicaoverfladerFigur 1. Skematisk diagram for 2-D numerisk model af CO 2 laserablation. Kredit:SIOM Smeltet silica er et vigtigt materiale til mange anvendelser inden for optik og fotonik på grund af dets frem
CO2 -laserablation fører en ny vej til skræddersyede kontinuerlige smeltede silicaoverfladerFigur 1. Skematisk diagram for 2-D numerisk model af CO 2 laserablation. Kredit:SIOM Smeltet silica er et vigtigt materiale til mange anvendelser inden for optik og fotonik på grund af dets frem -
 Finjustering af termoelektriske materialer til billigere vedvarende energiKredit:CC0 Public Domain Forskere fra Queen Mary University of London har udviklet nye termoelektriske materialer, som kunne give en billig mulighed for at omdanne varmeenergi til elektricitet. M
Finjustering af termoelektriske materialer til billigere vedvarende energiKredit:CC0 Public Domain Forskere fra Queen Mary University of London har udviklet nye termoelektriske materialer, som kunne give en billig mulighed for at omdanne varmeenergi til elektricitet. M
- Hvad er den enkleste organisation af stof?
- Hvad er ceramid?
- Sådan konverteres hestekræfter til mil pr. Time
- Hvad gnavere lever i Colorado?
- Hvis hyppigheden af en bølge, der kører i reb, er fordoblet, hvad vil der ske med hastighedsbøl…
- Hvad er massen, hvis kraft 10n og acceleration 2m sekund kvadratisk?


