Heliums inerthed:Hvorfor danner det sjældent forbindelser?
Her er hvorfor:
* Stabil elektronkonfiguration: Helium har to elektroner i sin yderste skal, hvilket er det maksimale, det kan holde. Denne komplette skal giver den en meget lav energitilstand, hvilket gør den ekstremt stabil.
* Høj ioniseringsenergi: Det kræver meget energi at fjerne en elektron fra helium, hvilket yderligere reducerer dens tendens til at deltage i kemiske reaktioner.
* Svage interatomiske kræfter: Heliumatomer danner ikke stærke bindinger med andre atomer på grund af deres mangel på elektronegativitet.
Selvom det er ekstremt svært at få helium til at danne forbindelser, har der været nogle teoretiske forudsigelser og endda et par eksperimentelle observationer tyder på muligheden for heliumforbindelser under ekstreme forhold. Disse er dog meget sjældne og ustabile, og helium forbliver stort set ureaktivt i de fleste situationer.
Opsummering: Heliums stabilitet på grund af dets fulde elektronskal og høje ioniseringsenergi gør det utroligt svært at danne forbindelser.
Sidste artikelHeliumforbindelser:Udforskning af undtagelserne for inerthed
Næste artikelBeregn pH:Løsning for surhed med [H+] =7,0 x 10^-12
 Varme artikler
Varme artikler
-
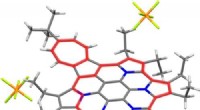 Dobbelt aromatiske ringe stabiliserer multikationerPyrrol- og azulenfusioneret azacoronen-dikering med 22π 6π aromatiske ringe. Kredit:American Chemical Society Et redoxaktivt polycyklisk aromatisk kulbrinte (PAHer) sammensat af azulen og pyrroler
Dobbelt aromatiske ringe stabiliserer multikationerPyrrol- og azulenfusioneret azacoronen-dikering med 22π 6π aromatiske ringe. Kredit:American Chemical Society Et redoxaktivt polycyklisk aromatisk kulbrinte (PAHer) sammensat af azulen og pyrroler -
 Gør stabile molekyler reaktive med lysBo Durbeej, professor i beregningsfysik ved Linköpings Universitet. Kredit:Thor Balkhed/Linköpings Universitet Forskere ved Linköpings Universitet har brugt computersimuleringer til at vise, at sta
Gør stabile molekyler reaktive med lysBo Durbeej, professor i beregningsfysik ved Linköpings Universitet. Kredit:Thor Balkhed/Linköpings Universitet Forskere ved Linköpings Universitet har brugt computersimuleringer til at vise, at sta -
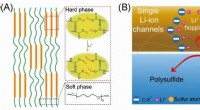 Stabiliserende svovlkatode med enkelt Li-ion-kanal polymerbindemiddel(A) Skematiske diagrammer over dannelsen af polymeren med enkeltionkanalerne. (B) Skematiske diagrammer af enkelt-ion-kanaler regulerer polysulfid- og Li-ion-hopningen. Kredit:©Science China Press
Stabiliserende svovlkatode med enkelt Li-ion-kanal polymerbindemiddel(A) Skematiske diagrammer over dannelsen af polymeren med enkeltionkanalerne. (B) Skematiske diagrammer af enkelt-ion-kanaler regulerer polysulfid- og Li-ion-hopningen. Kredit:©Science China Press -
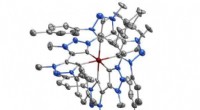 Moderne alkymi skaber selvlysende jernmolekylerKredit:Lunds Universitet En gruppe forskere ved Lunds Universitet i Sverige har lavet det første jernbaserede molekyle, der er i stand til at udsende lys. Dette kunne bidrage til udviklingen af
Moderne alkymi skaber selvlysende jernmolekylerKredit:Lunds Universitet En gruppe forskere ved Lunds Universitet i Sverige har lavet det første jernbaserede molekyle, der er i stand til at udsende lys. Dette kunne bidrage til udviklingen af
- Hvor meget olie har vi brugt?
- Hvad lærte Ernest Rutherford af sit guldfolieeksperiment?
- Omdannelse af absorberede fotoner med 2-oxocarboxylsyrer til yderst reaktivt singlet oxygen
- Hvorfor er det bedste eksempel på en pionerart, der ville blive fundet, hvor Glacier er trukket til…
- Er et vandfald dannet af erosion eller afsætning?
- Hvad er forskelligt af en bakterieceller fra dyre- og planterceller?


