Beregning af massen af ammoniumchlorid i en opløsning:en trin-for-trin guide
1. Forstå Molaritet
Molaritet (M) er en koncentrationsenhed, der fortæller dig antallet af mol opløst stof pr. liter opløsning.
2. Beregn mol af ammoniumchlorid
* Du har en 2,00 M opløsning, hvilket betyder, at der er 2,00 mol ammoniumchlorid (NH₄Cl) pr. liter opløsning.
* Du har 0,500 L opløsning.
* For at finde mol NH₄Cl skal du gange molariteten med volumen:
(2,00 mol/L) * (0,500 L) =1,00 mol NH4Cl
3. Konverter mol til gram
* Den molære masse af NH₄Cl er cirka 53,49 g/mol (du kan finde dette i det periodiske system).
* Multiplicer mol NH₄Cl med dens molære masse for at få massen i gram:
(1,00 mol) * (53,49 g/mol) =53,49 gram
Svar: Der er 53,49 gram ammoniumchlorid i 0,500 L af en 2,00 M opløsning.
 Varme artikler
Varme artikler
-
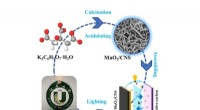 Carbon nanoark som en kompetent assistent til mangandioxid viser bemærkelsesværdig ydeevne i super…Kredit:Higher Education Press I forbindelse med kulstofneutralitet har superkondensatorer, som en ny grøn energilagringsenhed, vist fordele såsom hurtig opladning og afladning, høj effekttæthed og
Carbon nanoark som en kompetent assistent til mangandioxid viser bemærkelsesværdig ydeevne i super…Kredit:Higher Education Press I forbindelse med kulstofneutralitet har superkondensatorer, som en ny grøn energilagringsenhed, vist fordele såsom hurtig opladning og afladning, høj effekttæthed og -
 Feltforsøg viser, at nyt katalysatormateriale til elektrolysatorer er pålideligtForskerne Emiliana Fabbri og Thomas Schmidt i et laboratorium på PSI, hvor de gennemførte eksperimenter for at studere ydelsen af den nyudviklede katalysator til elektrolysatorer. Kredit:Paul Scherr
Feltforsøg viser, at nyt katalysatormateriale til elektrolysatorer er pålideligtForskerne Emiliana Fabbri og Thomas Schmidt i et laboratorium på PSI, hvor de gennemførte eksperimenter for at studere ydelsen af den nyudviklede katalysator til elektrolysatorer. Kredit:Paul Scherr -
 Kemikere udvikler urinprøve med papirstrimmel til evaluering derhjemme/på kontoret/klinikkenRobbyn Anand og studerende i hendes forskningsgruppe udvikler en ny papirstrimletest for at opdage coronavirus, der forårsager COVID-19. Kredit:College of Liberal Arts and Sciences Kemikere ved Io
Kemikere udvikler urinprøve med papirstrimmel til evaluering derhjemme/på kontoret/klinikkenRobbyn Anand og studerende i hendes forskningsgruppe udvikler en ny papirstrimletest for at opdage coronavirus, der forårsager COVID-19. Kredit:College of Liberal Arts and Sciences Kemikere ved Io -
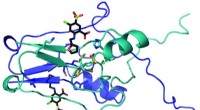 Forskere kortlægger krystaller for at fremme behandlinger for slagtilfælde, diabetes, demensEt hold af WVU-forskere – inklusive Werner Geldenhuys, John Hollander og Aaron Robart - har kortlagt krystalstrukturen af et protein kaldet mitoNEET og udpeget, hvordan et lægemiddel låser sig på de
Forskere kortlægger krystaller for at fremme behandlinger for slagtilfælde, diabetes, demensEt hold af WVU-forskere – inklusive Werner Geldenhuys, John Hollander og Aaron Robart - har kortlagt krystalstrukturen af et protein kaldet mitoNEET og udpeget, hvordan et lægemiddel låser sig på de
- Dinosaur blod? Ny forskning opfordrer til forsigtighed med hensyn til fossiliseret blødt væv
- Magnetiske nanopartikler bruges til at kontrollere tusindvis af celler samtidigt
- Hvad er de to skabsplaneter til Venus?
- Ingeniører opnår et betydeligt gennembrud inden for spin -wave -baseret informationsteknologi
- Apple laver iPhone 14 i Indien på skift væk fra Kina
- Video:Forberedelse af MetOp-C


