Svovlegenskaber:En omfattende guide til egenskaber og adfærd
Svovl:Karakteristika og egenskaber
Svovl er et fascinerende element med en række interessante egenskaber:
Fysiske egenskaber:
* Udseende: Et lysegult, lugtfrit, sprødt fast stof ved stuetemperatur.
* Smeltepunkt: 115,21 °C (239,38 °F)
* Kogepunkt: 444,6 °C (832,3 °F)
* Tæthed: 2,07 g/cm³ (fast)
* Opløselighed: Uopløseligt i vand, men opløseligt i kulstofdisulfid.
* Elektrisk ledningsevne: En dårlig leder af elektricitet.
* Krystalstruktur: Findes i forskellige krystallinske former, hvor rombisk svovl er det mest stabile ved stuetemperatur.
Kemiske egenskaber:
* Oxidationstilstande: Udviser en bred vifte af oxidationstilstande, fra -2 til +6.
* Reaktivitet: Reagerer med mange metaller, ikke-metaller og forbindelser.
* Brændbarhed: Brænder let i luft og producerer svovldioxid (SO2) gas, som har en skarp lugt.
* Surhed: Svovldioxid opløses i vand og danner svovlsyrling (H2SO3), en svag syre.
* Danning af sulfider: Reagerer med mange metaller og danner sulfider, som ofte er farvede forbindelser.
* Danning af sulfater: Oxideret til dannelse af sulfater, som er vigtige komponenter i mange mineraler og salte.
Andre bemærkelsesværdige egenskaber:
* Allotroper: Svovl findes i flere allotropiske former, herunder rombisk, monoklinisk og plastisk svovl.
* Biologisk betydning: Svovl er et essentielt element for livet, da det findes i aminosyrer, proteiner og enzymer.
* Industrielle anvendelser: Svovl bruges til fremstilling af svovlsyre, et vigtigt industrikemikalie, såvel som til fremstilling af gødning, gummi og rengøringsmidler.
* Miljøeffekter: Svovldioxidemissioner kan bidrage til sur regn og luftvejsproblemer.
Opsummering:
Svovl er et alsidigt grundstof med unikke kemiske og fysiske egenskaber. Det spiller en afgørende rolle i industrielle processer, miljøkemi og biologiske systemer. Dens evne til at danne en bred vifte af forbindelser gør den til et væsentligt element i mange aspekter af vores liv.
Sidste artikelIdentifikation af dårlige elektriske ledere:Ilt, zink og jod
Næste artikelSvovlegenskaber:Fysiske og kemiske egenskaber
 Varme artikler
Varme artikler
-
 Forskere bringer polymerer i fokus på atomskalaEn gengivelse (grå og pink) af den molekylære struktur af en peptoid polymer, der blev undersøgt af et team ledet af Berkeley Lab og UC Berkeley. Holdets succes med at afbilde polymerers struktur i at
Forskere bringer polymerer i fokus på atomskalaEn gengivelse (grå og pink) af den molekylære struktur af en peptoid polymer, der blev undersøgt af et team ledet af Berkeley Lab og UC Berkeley. Holdets succes med at afbilde polymerers struktur i at -
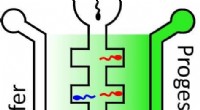 En ny måde at vurdere mandlig fertilitet påMere sædceller bevæger sig til højre side af en central kanal, som indeholder høje koncentrationer af progesteron (mørkegrøn), end til venstre side, som indeholder lavere koncentrationer (lysegrøn). K
En ny måde at vurdere mandlig fertilitet påMere sædceller bevæger sig til højre side af en central kanal, som indeholder høje koncentrationer af progesteron (mørkegrøn), end til venstre side, som indeholder lavere koncentrationer (lysegrøn). K -
 Sådan identificeres bøjede molekylære geometrier ved hjælp af VSEPRAf Scott Becker Opdateret 30. august 2022 Molekylær form kan forudsiges med Valence Shell Electron Pair Repulsion (VSEPR) modellen, et grundlæggende værktøj, der undervises i avancerede kemikurser v
Sådan identificeres bøjede molekylære geometrier ved hjælp af VSEPRAf Scott Becker Opdateret 30. august 2022 Molekylær form kan forudsiges med Valence Shell Electron Pair Repulsion (VSEPR) modellen, et grundlæggende værktøj, der undervises i avancerede kemikurser v -
 Nye molekyler kan bruges til at behandle autoimmune sygdomme i fremtidenKredit:Bart van Overbeeke Når noget er galt med dit immunsystem, din fordøjelse eller dine endokrine systemer nukleare receptorer, som de kaldes, godt kan være involveret. Hvis det er nødvendigt,
Nye molekyler kan bruges til at behandle autoimmune sygdomme i fremtidenKredit:Bart van Overbeeke Når noget er galt med dit immunsystem, din fordøjelse eller dine endokrine systemer nukleare receptorer, som de kaldes, godt kan være involveret. Hvis det er nødvendigt,
- Ny hulkrystal rydder en vej for kvantelys
- Hvordan afbalancerer du al plus cl cu?
- Hvad kaldes en celle, der ikke har nogen kerne?
- Hvad er nogle menneskelige miljøinteraktioner i Cuba?
- Hvis to organismer ligner meget ens i deres tidlige udviklingsstadier, er dette bevis for, at det er…
- Forskere opdager skjult kammer i Egyptens store pyramide


