Sådan identificeres bøjede molekylære geometrier ved hjælp af VSEPR
Af Scott Becker
Opdateret 30. august 2022
Molekylær form kan forudsiges med Valence Shell Electron Pair Repulsion (VSEPR) modellen, et grundlæggende værktøj, der undervises i avancerede kemikurser verden over. VSEPR overvejer antallet af bindingssteder og ensomme par omkring et centralt atom for at forudsige et molekyles geometri. En "bøjet" form opstår, når et centralt atom har to bindingssteder og et eller to ensomme par. Ved at anvende VSEPR-principperne kan du pålideligt afgøre, om et molekyle antager en bøjet konfiguration.
Trin 1
Skriv den kemiske formel for molekylet ned (f.eks. HF, NO).
Trin 2
Beregn det samlede antal valenselektroner ved hjælp af det periodiske system. For vejledning henvises til afsnittet Ressourcer om elektrontælling.
Trin 3
Tegn Lewis-strukturen:brug enkelte linjer til bindinger og prikker til enlige elektroner. Husk, at hver binding bidrager med to elektroner, og det samlede antal elektroner i strukturen skal svare til antallet fra trin 2.
Trin 4
Identificer det centrale atom og tæl dets bindingssteder plus enlige elektronpar – dette er det steriske tal.
Trin 5
Analyser det steriske tal:en bøjet geometri kræver et sterisk tal på 3 eller 4 med mindst ét ensomt par. Hvis antallet afviger, er molekylet ikke bøjet.
Trin 6
Se et VSEPR-diagram (se Ressourcer) for at matche sterisk tal, bindingssteder og ensomme par til den forudsagte molekylære form.
TL;DR (for lang; læste ikke)
Når du tegner Lewis-strukturen, hvis elektrontallet er slået fra, skal du justere ved at tilføje dobbelt- eller tredobbeltbindinger og fjerne enlige par efter behov for at opnå en afbalanceret struktur.
 Varme artikler
Varme artikler
-
 Hele forestillingen, intet af balladen:nitrilhydrogenering udført rigtigtFigur 1:Katalytisk hydrogenering af nitriler til primære aminer. Kredit:Osaka University Behovet for at være opmærksomme forbrugere er ved at blive en prioritet for en stadigt voksende del af samf
Hele forestillingen, intet af balladen:nitrilhydrogenering udført rigtigtFigur 1:Katalytisk hydrogenering af nitriler til primære aminer. Kredit:Osaka University Behovet for at være opmærksomme forbrugere er ved at blive en prioritet for en stadigt voksende del af samf -
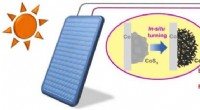 Ny elektrokatalysator udviklet til biomasseopgradering og brintgenereringDen fotovoltaiske elektrokatalyse til biomasseopgradering og brintgenerering. Kredit:NIMTE Prof. Zhang Jians team ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under det kine
Ny elektrokatalysator udviklet til biomasseopgradering og brintgenereringDen fotovoltaiske elektrokatalyse til biomasseopgradering og brintgenerering. Kredit:NIMTE Prof. Zhang Jians team ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under det kine -
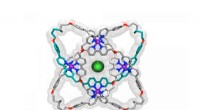 Molekylær knude vinder rekord for verdens strammesteRøntgenkrystalstruktur af en molekylær knude med otte krydsninger. Kredit:Jean-Francois Lemonnier, University of Manchester Forskere ved University of Manchester fejrer efter at være blevet rekord
Molekylær knude vinder rekord for verdens strammesteRøntgenkrystalstruktur af en molekylær knude med otte krydsninger. Kredit:Jean-Francois Lemonnier, University of Manchester Forskere ved University of Manchester fejrer efter at være blevet rekord -
 Fotosyntese:Redox-processen, der opretholder livetAf Kevin Beck, Opdateret 30. august 2022 James ONeil/DigitalVision/GettyImages Fotosyntese er den fundamentale biokemiske kaskade, der driver livet på Jorden. Selvom kun en undergruppe af organismer
Fotosyntese:Redox-processen, der opretholder livetAf Kevin Beck, Opdateret 30. august 2022 James ONeil/DigitalVision/GettyImages Fotosyntese er den fundamentale biokemiske kaskade, der driver livet på Jorden. Selvom kun en undergruppe af organismer
- Nye data viser et stærkt arbejdsmarked for forskere og ingeniører
- Hvad er de vigtigste årsager til forvitring af erosion og aflejring?
- Hvad er de første organismer, der besætter et golde landskab efter en begivenhed som glacial?
- Hvilken slags fysisk mængde er en længde?
- Videnskabshyrder Perseverance rover gennem første fase af Mars stenprøvetagning
- Din solcreme forurener måske havet – men alger kan være et naturligt alternativ


