Beregning af masseprocenten af vandfrit kobbersulfat i CuSO4·5H2O
Af Jack Brubaker
Opdateret 30. august 2022
Kobbersulfatpentahydrat (CuSO4·5H2O) er et hydrat, hvilket betyder, at vandmolekylerne er kemisk bundet til det vandfri salt. En prøve på 100 gram af hydratet indeholder derfor både kobbersulfat og vand. For at udtrykke, hvor meget kobbersulfat der er til stede, bruger kemikere masseprocenten (masseprocent) af den vandfri komponent.
Trin 1 – Bestem formelvægten af CuSO4·5H2O
Brug standard atomvægte (IUPAC), beregn massen af hvert element i formlen og summer dem:
- Cu = 63,55amu × 1 = 63,55amu
- S = 32.07amu × 1 = 32.07amu
- O = 16.00amu × 9 = 144.00amu
- H = 1,01amu × 10 = 10,10amu
Formelvægt = 63,55 + 32,07 + 144,00 + 10,10 = 249,72 amu.
Trin 2 – Bestem formelvægten af vandfrit CuSO4
Fjern vandbidraget:
- Cu = 63,55amu × 1 = 63,55amu
- S = 32.07amu × 1 = 32.07amu
- O = 16.00amu × 4 = 64.00amu
Formelvægt = 63,55 + 32,07 + 64,00 = 159,62 amu.
Trin 3 – Beregn masseprocenten af CuSO4
Divider den vandfri vægt med hydratvægten og gang med 100 %:
159,62/249,72 × 100 ≈ 63,92 %
En prøve på 100 gram af kobbersulfatpentahydrat indeholder således omkring 63,92 g CuSO4 og 36,08 g vand.
Nødvendige materialer
- Periodisk tabel over elementerne
- Videnskabelig lommeregner
TL;DR
Brug atomvægtene til at beregne formelvægtene for CuSO4·5H2O og CuSO4, divider og multiplicer derefter med 100 for at opnå masseprocenten af vandfrit kobbersulfat (≈63,9%).
 Varme artikler
Varme artikler
-
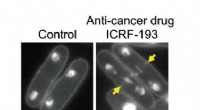 Anticancer-mekanisme afsløret i gæreksperimenterMed DNA topoisomerase II (topo II) intakt, DNA i fissionsgærceller replikeres normalt og deles jævnt mellem to datterceller (venstre). Når det er under virkningen af anti-cancer lægemidlet ICRF-193,
Anticancer-mekanisme afsløret i gæreksperimenterMed DNA topoisomerase II (topo II) intakt, DNA i fissionsgærceller replikeres normalt og deles jævnt mellem to datterceller (venstre). Når det er under virkningen af anti-cancer lægemidlet ICRF-193, -
 Forskere opnår nye resultater i undersøgelsen af uorganiske pigmenter med apatitstrukturPrøve af høj renhed af bariumhypomanganatchlorid. Kredit:Lobachevsky University Forbindelser med apatitstrukturen adskiller sig fra de fleste klasser ved de forskellige kemiske sammensætninger. Fo
Forskere opnår nye resultater i undersøgelsen af uorganiske pigmenter med apatitstrukturPrøve af høj renhed af bariumhypomanganatchlorid. Kredit:Lobachevsky University Forbindelser med apatitstrukturen adskiller sig fra de fleste klasser ved de forskellige kemiske sammensætninger. Fo -
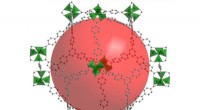 Kemikere udvikler rekordstort porøst krystallinsk materiale med verdens højeste overfladearealSkelet på DUT-60 har et porevolumen på 5,02 cm3g-1 - det højeste specifikke porevolumen, man nogensinde har målt blandt alle krystallinske rammematerialer hidtil. Kredit:Dr. I. Senkovska, TU Dresden
Kemikere udvikler rekordstort porøst krystallinsk materiale med verdens højeste overfladearealSkelet på DUT-60 har et porevolumen på 5,02 cm3g-1 - det højeste specifikke porevolumen, man nogensinde har målt blandt alle krystallinske rammematerialer hidtil. Kredit:Dr. I. Senkovska, TU Dresden -
 En katalytisk balancegang for opdeling af vand i hydrogen og iltArgonne -forskere og deres samarbejdspartnere har brugt en ny og kontraintuitiv tilgang til at afbalancere tre vigtige faktorer - aktivitet, stabilitet og ledningsevne - i en ny katalysator designet t
En katalytisk balancegang for opdeling af vand i hydrogen og iltArgonne -forskere og deres samarbejdspartnere har brugt en ny og kontraintuitiv tilgang til at afbalancere tre vigtige faktorer - aktivitet, stabilitet og ledningsevne - i en ny katalysator designet t
- Hvordan ødelægger mennesker bjerge?
- Den næste store ting:Hvordan bringer videnskabsmænd brintbrændselsceller fra laboratoriet til det…
- Nanobowls serverer kemoterapi til kræftceller
- Hvordan ændrer statisk elektricitet gebyrerne for et objekt?
- Hvordan ligner en celle fabriksliste mindst 5 ligheder?
- Hvordan adskiller du svovl fra rulle svovl og kulstof?


