Forståelse af aktiveringsenergi i jod-urreaktionen
Af Jack Brubaker, opdateret 30. august 2022
Billedkredit:Apiwan Borrikonratchata/iStock/GettyImages
Jod-ur-reaktionen er en klassisk demonstration, der bruges af gymnasieelever og kemistuderende til at visualisere principperne for kemisk kinetik. I denne reaktion oxiderer hydrogenperoxid iodid til jod. Jodet reagerer derefter med thiosulfat, indtil thiosulfatet er forbrugt. Når thiosulfatet er opbrugt, gør en stivelsesindikator opløsningen til en dyb blå farve, hvilket markerer tidspunktet for "uret".
Hvad er aktiveringsenergi?
Enhver kemisk transformation kræver brydning af bindinger i reaktanterne. Den energi, der skal tilføres for at nå denne overgangstilstand, er kendt som aktiveringsenergien (Ea). Mens en reaktion kan være termodynamisk gunstig – producerer produkter med lavere samlet energi – er reaktionshastigheden styret af Ea.
Sådan måler du aktiveringsenergi
For at bestemme Ea måler man hastighedskonstanten (k) ved flere temperaturer. Plotning af den naturlige logaritme af k mod den reciproke af den absolutte temperatur (1/T, med T i Kelvin) skulle producere en ret linje. Hældningen af denne linje er lig med –Ea/R, hvor R er den ideelle gaskonstant (8,314 Jmol⁻¹K⁻¹).
Aktiveringsenergi af jod-ur-reaktionen
For jod-ur-systemet giver lnk versus 1/T plottet en hældning på cirka –6230. Brug af forholdet –Ea/R=–6230 giver en aktiveringsenergi på omkring 51,8kJmol⁻¹ (51800Jmol⁻¹). Denne værdi afspejler den energibarriere, der skal overvindes, for at iodidoxidationen og det efterfølgende thiosulfatforbrug kan fortsætte.
 Varme artikler
Varme artikler
-
 Omdannelse af gas til brændstoffer med bedre legeringerAfbildet, platin-kobber enkeltatom legeringen. Kobber (orange) er ude af stand til at bryde bindinger mellem kulstof (sort) og brint (klart) i metanderivater undtagen ved højere temperaturer, men et e
Omdannelse af gas til brændstoffer med bedre legeringerAfbildet, platin-kobber enkeltatom legeringen. Kobber (orange) er ude af stand til at bryde bindinger mellem kulstof (sort) og brint (klart) i metanderivater undtagen ved højere temperaturer, men et e -
 Tæller perovskitterGlasrør med kvanteprikker af perovskit -nanokrystaller, lysende med alle regnbuens farver under ultraviolet stråling. Kredit:Shutterstock Marina Filip, Postdoktoral forskningsassistent, og Felicia
Tæller perovskitterGlasrør med kvanteprikker af perovskit -nanokrystaller, lysende med alle regnbuens farver under ultraviolet stråling. Kredit:Shutterstock Marina Filip, Postdoktoral forskningsassistent, og Felicia -
 Computermodel til design af proteinsekvenser, der er optimeret til at binde til lægemiddelmålVed at bruge en computermodelleringstilgang, som de udviklede, MIT-biologer identificerede tre forskellige proteiner, der kan binde selektivt til hver af tre lignende mål, alle medlemmer af Bcl-2-fami
Computermodel til design af proteinsekvenser, der er optimeret til at binde til lægemiddelmålVed at bruge en computermodelleringstilgang, som de udviklede, MIT-biologer identificerede tre forskellige proteiner, der kan binde selektivt til hver af tre lignende mål, alle medlemmer af Bcl-2-fami -
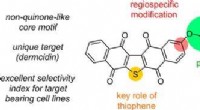 Havvandsbakterier giver fører til bekæmpelse af melanomKredit:American Chemical Society Malignt melanom kan være en særlig farlig form for kræft, og flere terapeutiske muligheder er nødvendige. Nu, forskere rapporterer i ACS Medicinal Chemistry Lette
Havvandsbakterier giver fører til bekæmpelse af melanomKredit:American Chemical Society Malignt melanom kan være en særlig farlig form for kræft, og flere terapeutiske muligheder er nødvendige. Nu, forskere rapporterer i ACS Medicinal Chemistry Lette
- Hvad er anderledes ved det astronomiske legeme af planeten Merkur?
- Hvilke arter er de øverste forbrugere af biosfæren?
- Ny rejse til universet fra DESHIMA
- Mastering Ratio Scaling:Sådan forstørres og forenkles forhold
- Hvorfor går en elektron i et kaliumatom det fjerde energiniveau i stedet for at klemme ind på tred…
- Hvad sker der, når du har divergerende grænser ved ubådudbrud og indtrængen af rhyolitisk magm…


