Trin-for-trin guide:Syntetisering af sølvoxid fra sølvnitrat
Af Alec Tasi | Opdateret 30. august 2022
Mens sølvs metalliske glans er dens mest berømte egenskab, er dens kemi lige så fascinerende. Et af de mest almindelige laboratoriepræparater involverer omdannelse af sølvnitrat til sølvoxid (Ag₂O), en forbindelse med anvendelser lige fra kulstofskrub til batteriteknologi og antimikrobielle belægninger. Den overordnede reaktion er:
2 AgNO₃(aq) + 2 NaOH(aq) → Ag₂O(s) + 2 NaNO₃(aq) + H₂O(l)
Sikkerhed først
Sølvnitrat er stærkt ætsende og kan forårsage hudforbrændinger eller permanent misfarvning. Natriumhydroxid er et stærkt irriterende stof. Brug opløsninger med lav molaritet, og brug altid handsker, sikkerhedsbriller og en laboratoriefrakke. Bortskaf alt affald i en forseglet beholder som instrueret i lokale retningslinjer for farligt affald.
Materialer
- Hansker (kemisk-resistente)
- Reagensglas og reagensglasstativ
- Pipette (20 mL kapacitet)
- 0,1 M sølvnitrat (AgNO₃)
- 0,5 M natriumhydroxid (NaOH)
- Deioniseret vand
- Bægerglas
- Tang
- Bunsenbrænder med gnister
Procedure
Trin 1 – Forberedelse
Tag handsker på og skyl reagensglasset med deioniseret vand. Fastgør den i stativet.
Trin 2 – Blanding
Brug pipetten til at overføre 20 mL 0,1 M sølvnitrat til reagensglasset. Skyl pipetten grundigt med deioniseret vand, og tilsæt derefter 20 mL 0,5 M natriumhydroxid. Der skulle straks komme et brunt bundfald.
Trin 3 – Afregning
Lad blandingen stå i 20 minutter, eller indtil det brune bundfald har bundfældet sig helt i bunden. Vip forsigtigt røret for at bekræfte, at det faste stof har fjernet væsken.
Trin 4 – Isolering
Dekanter forsigtigt supernatanten (natriumnitratopløsning) i et bægerglas, så den faste Ag₂O-klump efterlades i reagensglasset. Forsegl affaldsopløsningen for sikker bortskaffelse.
Trin 5 – Tørring
Tænd Bunsen-brænderen med gnisten. Brug en tang til at holde reagensglasset et par centimeter fra flammen for langsomt at fjerne resterende vanddamp, hvilket giver tørt sølvoxidpulver.
Nøglepunkter at huske
• Udsæt ikke reagensglasset for kraftig varme; Ag₂O nedbrydes over ~300°C.
• Alle reagenser skal håndteres i et godt ventileret område.
• Indtag eller tillad aldrig kontakt med huden; vask grundigt, hvis der opstår utilsigtet kontakt.
Anvendelser af sølvoxid
Sølvoxids redoxegenskaber gør det værdifuldt som kulskrubber, en komponent i sølvoxidbatterier og en antimikrobiel overfladebehandling.
 Varme artikler
Varme artikler
-
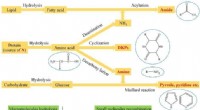 En ny idé til raffinering af bioråolieKredit:Bao et al., Grænser for kemividenskab og ingeniørvidenskab (2022). DOI:10.1007/s11705-021-2126-y Det høje indhold af nitrogenholdige organiske forbindelser (NOCer) i biocrude opnået fra hydr
En ny idé til raffinering af bioråolieKredit:Bao et al., Grænser for kemividenskab og ingeniørvidenskab (2022). DOI:10.1007/s11705-021-2126-y Det høje indhold af nitrogenholdige organiske forbindelser (NOCer) i biocrude opnået fra hydr -
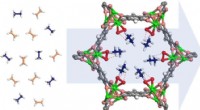 Nyt materiale kunne gøre plastikfremstilling mere energieffektivDenne jernbaserede metal-organiske ramme dekoreret med peroxo-grupper (røde og grønne) kan fange ethan (blå molekyler), mens den tillader ethylen (ferskenmolekyler) at passere igennem, potentielt give
Nyt materiale kunne gøre plastikfremstilling mere energieffektivDenne jernbaserede metal-organiske ramme dekoreret med peroxo-grupper (røde og grønne) kan fange ethan (blå molekyler), mens den tillader ethylen (ferskenmolekyler) at passere igennem, potentielt give -
 Kemisk innovation stabiliserer den bedst ydende perovskit-formuleringUdgiver i Videnskab , forskere ved EPFL har med succes overvundet et begrænsende problem med at stabilisere den bedst ydende formulering af metalhalogenid perovskitfilm, en nøglespiller i en række a
Kemisk innovation stabiliserer den bedst ydende perovskit-formuleringUdgiver i Videnskab , forskere ved EPFL har med succes overvundet et begrænsende problem med at stabilisere den bedst ydende formulering af metalhalogenid perovskitfilm, en nøglespiller i en række a -
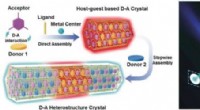 Heterostrukturkrystaller kunne lyse vejen til optiske kredsløbKredit:Wiley-VCH Det kan være muligt at nå nye niveauer af miniaturisering, hastighed, og databehandling med optiske kvantecomputere, som bruger lys til at transportere information. For det, vi ha
Heterostrukturkrystaller kunne lyse vejen til optiske kredsløbKredit:Wiley-VCH Det kan være muligt at nå nye niveauer af miniaturisering, hastighed, og databehandling med optiske kvantecomputere, som bruger lys til at transportere information. For det, vi ha
- Katalysator åbner døren til mere effektiv, miljøvenlig produktion af ethylen
- Et naturligt værktøj til at tackle olieudslip?
- China Mobile blokeret fra at tilbyde telefonservice i USA
- Hvad er to slags vinderosion?
- Hvad er en videnskabelig sætning for fejl i geologi?
- Hvilken rolle spillede tyngdekraften i dannelsen af solen?


