Hvordan man hurtigt bestemmer graden af umættethed i organiske molekyler
Apiwan Borrikonratchata/iStock/GettyImages
I organisk kemi indeholder en "umættet" forbindelse mindst én "pi"-binding - en dobbeltbinding mellem to carbonatomer, der bruger to elektroner fra hver carbon. At bestemme, hvor mange pi-bindinger en umættet forbindelse har - "umættethedsgraden" - kan være kedeligt, hvis du prøver at tegne molekylet manuelt. Ved at anvende en enkel, udbredt formel kan kemikere beregne dette tal på sekunder.
Trin 1 – Udskift halogener med hydrogener
Til beregningen behandles eventuelle halogener (brom, jod, klor osv.) som hydrogener. For eksempel, hvis din forbindelse er C6H6N3OCl , omskriv det som C6H7N3O .
Trin 2 – Se bort fra iltatomer
Iltatomer påvirker ikke graden af umættethed, så udelad dem. Eksemplet bliver C6H7N3 .
Trin 3 – Træk et brint fra pr. nitrogen fra
Hvert nitrogenatom reducerer effektivt brinttallet med én. Således C6H7N3 er forenklet til C6H4 .
Trin 4 – Anvend umættethedsformlen
Med molekylet nu i formen CnHm , beregn graden af umættethed vha. Ω =n – (m/2) + 1, hvor Ω er antallet af pi-bindinger og ringe. For eksempel:Ω =6 – (4/2) + 1 =6 – 2 + 1 =5. Derfor C6H6N3OCl indeholder fem dobbeltbindinger eller ringækvivalenter.
Denne enkle metode, der undervises i standardkurser i organisk kemi, giver en hurtig og pålidelig måde at vurdere umættetheden af ethvert organisk molekyle på.
 Varme artikler
Varme artikler
-
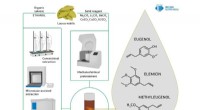 Kemikere forbedrer metoden til at udvinde naturlige antioxidanter fra laurbærbladeKredit:RUDN Universitet En kemiker fra RUDN Universitet og hans kolleger har foreslået at bruge rester fra forarbejdning af laurbærblade som råmateriale til fremstilling af kemisk aktive stoffer,
Kemikere forbedrer metoden til at udvinde naturlige antioxidanter fra laurbærbladeKredit:RUDN Universitet En kemiker fra RUDN Universitet og hans kolleger har foreslået at bruge rester fra forarbejdning af laurbærblade som råmateriale til fremstilling af kemisk aktive stoffer, -
 Kører du højt? Kemikere gør fremskridt mod marihuana-åndedrætsanalysatorForskernes THC-drevne brændselscellesensor med sit H-formede glaskammer. Kredit:Evan Darzi En kemiker fra UCLA og kolleger er nu et skridt nærmere deres mål om at udvikle et håndholdt værktøj, der
Kører du højt? Kemikere gør fremskridt mod marihuana-åndedrætsanalysatorForskernes THC-drevne brændselscellesensor med sit H-formede glaskammer. Kredit:Evan Darzi En kemiker fra UCLA og kolleger er nu et skridt nærmere deres mål om at udvikle et håndholdt værktøj, der -
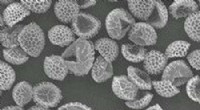 Rengøring af forurenende stoffer fra vand med pollen og sporer - uden achoo!De fyldte overflader af behandlede sporkorn, her vist forstørret cirka 300 gange, kan fjerne uønskede kemikalier fra forurenet vand. Kredit:Andrew Boa og Aimilia Meichanetzoglou Ud over deres roll
Rengøring af forurenende stoffer fra vand med pollen og sporer - uden achoo!De fyldte overflader af behandlede sporkorn, her vist forstørret cirka 300 gange, kan fjerne uønskede kemikalier fra forurenet vand. Kredit:Andrew Boa og Aimilia Meichanetzoglou Ud over deres roll -
 Forskere gør fremskridt inden for kontrol af kamæleonlignende materiale til næste generations com…Kredit:Texas A&M University Forskere fra Texas A&M University rapporterer om betydelige fremskridt i deres forståelse og kontrol af et kamæleonlignende materiale, der kan være nøglen til næste gen
Forskere gør fremskridt inden for kontrol af kamæleonlignende materiale til næste generations com…Kredit:Texas A&M University Forskere fra Texas A&M University rapporterer om betydelige fremskridt i deres forståelse og kontrol af et kamæleonlignende materiale, der kan være nøglen til næste gen
- Hvad kalder du en videnskabsmand, der studerer kurer for sygdomme?
- Hvordan kan videnskab bruges i fysik?
- Hvad er Genotype for Roan Color?
- Zink:Det perfekte materiale til bioabsorberbare stents?
- Definer en mol af et stof, der påføres atomstruktur?
- Et langt opviklet rør, hvor mad fordøjes og absorberes?


