Beregning af molaritet i titrering:En trin-for-trin guide
Af RussellL • Opdateret 30. august 2022
Titrering er en pålidelig analytisk teknik, der bruges til at bestemme koncentrationen af en ukendt opløsning ved at reagere den med et reagens af kendt koncentration. Reaktionens slutpunkt er identificeret ved en farveændring, pH-skift eller anden fysisk indikator, hvilket muliggør præcis beregning af det ukendtes molaritet.
Trin 1 – Beregn mol af standarden
Multiplicer titrantens molaritet (M) med dens volumen (V, i liter). Produktet giver det samlede antal mol af standardopløsningen:
n₁ = M₁ × V₁
Trin 2 – Identificer syre/base-støkiometrien
Undersøg formlen for analytten for at bestemme, hvor mange H⁺ (for syrer) eller OH⁻ (for baser) der frigives pr. molekyle. Dette heltal, n , fås direkte fra abonnenterne.
Trin 3 – Beregn Moles of the Unknown
Divider standardens mol med den støkiometriske faktor:
n₂ = n₁ ÷ n
Trin 4 – Udled molariteten af det ukendte
Til sidst divideres mol af analytten med dens volumen (V₂, i liter):
M₂ = n₂ ÷ V₂
Når den udføres korrekt, giver denne sekvens en nøjagtig molaritet for den ukendte opløsning.
 Varme artikler
Varme artikler
-
 Mestre stærke syrer og baser:Gennemprøvede hukommelsesteknikker til eksamenAf Claire Gillespie Opdateret 24. marts 2022 Slonme/iStock/GettyImages Hvis du skal huske navnene på stærke syrer og baser til en kemi-eksamen, skal du ikke gå i panik. Hvis simpel gentagelse ikke
Mestre stærke syrer og baser:Gennemprøvede hukommelsesteknikker til eksamenAf Claire Gillespie Opdateret 24. marts 2022 Slonme/iStock/GettyImages Hvis du skal huske navnene på stærke syrer og baser til en kemi-eksamen, skal du ikke gå i panik. Hvis simpel gentagelse ikke -
 Forsker arbejder på at forstå, hvordan gonoré udvikler resistens over for antibiotikaDette billede genereret ved røntgenkrystallografi viser et cephalosporin-antibiotikum, i pink, binding til et protein fra bakterien, der forårsager gonoré. Kuglerne repræsenterer vandmolekyler. Kredit
Forsker arbejder på at forstå, hvordan gonoré udvikler resistens over for antibiotikaDette billede genereret ved røntgenkrystallografi viser et cephalosporin-antibiotikum, i pink, binding til et protein fra bakterien, der forårsager gonoré. Kuglerne repræsenterer vandmolekyler. Kredit -
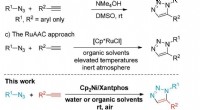 Team præsenterer ny syntesemetode til klikkemiSammenligningen af den eksisterende syntesemetode og den nyudviklede syntesemetode af professor Hong. Kredit:UNIST En nylig undersøgelse foretaget af forskere tilknyttet UNIST har præsenteret en
Team præsenterer ny syntesemetode til klikkemiSammenligningen af den eksisterende syntesemetode og den nyudviklede syntesemetode af professor Hong. Kredit:UNIST En nylig undersøgelse foretaget af forskere tilknyttet UNIST har præsenteret en -
 Sojamikroperler er miljøvenlige alternativer til plastmikroperler, der bruges i kosmetik, sæbe pro…Et team på fire nyuddannede i Purdue har udviklet SoyFoliate, en sojamikroperle-teknologi, der kunne tjene som et alternativ til de nyligt forbudte plastikmikroperler, der ofte findes i kosmetiske pro
Sojamikroperler er miljøvenlige alternativer til plastmikroperler, der bruges i kosmetik, sæbe pro…Et team på fire nyuddannede i Purdue har udviklet SoyFoliate, en sojamikroperle-teknologi, der kunne tjene som et alternativ til de nyligt forbudte plastikmikroperler, der ofte findes i kosmetiske pro
- Kan en kvasar udslette en hel planet?
- Hvor kan du finde isolatorer i nærheden af en kraftledning?
- Hvilken tilstand af stof har et bestemt volumen, men ingen form?
- Erosion afdækker knogler på New Yorks dødeø
- Når en enkelt celle gennemgår mange mitotiske opdelinger i kernen, der producerer datterceller, ha…
- Hvilken planet er flad form på grund af den meget hurtige rotation?


