Bestemmelse af reaktantrester i kemiske produkter:en trin-for-trin guide
Af Sean Lancaster , Opdateret Aug302022
I enhver kemisk syntese afhænger renheden af slutproduktet af, hvor meget af udgangsmaterialerne, der forbliver uomsat. Bestemmelse af det forventede udbytte kræver identifikation af den begrænsende reaktant og beregning af massen af overskydende reaktanter, der forbliver i produktet.
Trin 1:List reaktanterne
Skriv hvert stof ned, der deltager i den balancerede ligning. Disse er de eneste arter, der kan forblive i det færdige produkt.
Trin 2:Beregn molekylvægte
Sum atomvægtene af hvert grundstof i en reaktant. For eksempel:
- HCl :1.008+35.453=36.461gmol‑1
- CaCO₃ :40.078+12.011+3×15.999=100.086gmol‑1
Trin 3:Bestem molforholdet
Fra den afbalancerede ligning kan du læse, hvor mange mol af hver reaktant, der skal til. Til reaktionenCaCO₃ + 2HCl → CaCl2 + CO₂ + H2O :
- 1 mol CaCO₃ kræver 2mol HCl (forhold 1:2)
- 1 mol HCl kræver ½ mol CaCO₃ (forhold 1:½)
Trin 4:Identificer det begrænsende reagens
Konverter startmasserne til mol (masse ÷ molekylvægt). I vores eksempel:
- 30,027 g CaCO₃ ÷ 100,086 gmol‑1 =0,300 mol
- 10,938 g HCl ÷ 36,461 gmol‑1 =0,478 mol
Trin 5:Beregn overskydende reaktant
Bestem, hvor meget af den ikke-begrænsende reaktant, der er tilbage efter reaktionen. 0,478 mol HCl har brug for 0,239 mol CaCO₃ for at reagere fuldstændigt. Overskydende CaCO₃ =0,300–0,239=0,061 mol.
Trin 6:Konverter overskydende til gram
Multiplicer de overskydende mol med molekylvægten:0,061 mol × 100,086 gmol‑1 ≈6,10 g CaCO₃ tilbage i produktet.
Værktøjer, du skal bruge
- Periodisk tabel (for atomvægte)
- Balanceret kemisk ligning
- Videnskabelig lommeregner
Ved at følge disse trin kan du nøjagtigt kvantificere ureagerede arter, så du kan designe oprensninger, der opnår den ønskede produktrenhed.
 Varme artikler
Varme artikler
-
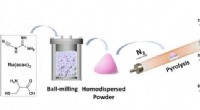 Nye enkelt-atom katalyse støvler reduktiv amineringsreaktionSkematisk illustration til fremstilling af Ru1/NC-T katalysatorer. Kredit:DICP Den geometriske isolering af metalarter i single-atom catalyse (SACer) maksimerer ikke kun atomudnyttelseseffektivite
Nye enkelt-atom katalyse støvler reduktiv amineringsreaktionSkematisk illustration til fremstilling af Ru1/NC-T katalysatorer. Kredit:DICP Den geometriske isolering af metalarter i single-atom catalyse (SACer) maksimerer ikke kun atomudnyttelseseffektivite -
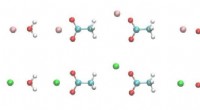 Force field analyse giver spor til protein-ion interaktionStrukturer af metalion-ligand-dimerer. Hvid, cyan, blå, rød, lyserøde og grønne kugler er H, C, N, O, Mg- og Ca -atomer. Kredit:Zhifeng Jing, Rui Qi, Chengwen Liu og Pengyu Ren Muskel rykninger, f
Force field analyse giver spor til protein-ion interaktionStrukturer af metalion-ligand-dimerer. Hvid, cyan, blå, rød, lyserøde og grønne kugler er H, C, N, O, Mg- og Ca -atomer. Kredit:Zhifeng Jing, Rui Qi, Chengwen Liu og Pengyu Ren Muskel rykninger, f -
 Mikrostruktureret materiale med rumlig variation har kun friktion i én retningEn sammenligning mellem ensartede funktioner (type 1), venstre, og en gruppe funktioner, der udviser envejsfriktion (type 2), ret, med resulterende kraft-rum-plots, der viser ydeevne, bund. I neutral
Mikrostruktureret materiale med rumlig variation har kun friktion i én retningEn sammenligning mellem ensartede funktioner (type 1), venstre, og en gruppe funktioner, der udviser envejsfriktion (type 2), ret, med resulterende kraft-rum-plots, der viser ydeevne, bund. I neutral -
 Nyt kompositmateriale, der kan køle sig selv ned under ekstreme temperaturerKredit:CC0 Public Domain Et banebrydende materiale, inspireret af naturen, der kan regulere sin egen temperatur og ligeså kunne bruges til at behandle forbrændinger og hjælpe rumkapsler til at mod
Nyt kompositmateriale, der kan køle sig selv ned under ekstreme temperaturerKredit:CC0 Public Domain Et banebrydende materiale, inspireret af naturen, der kan regulere sin egen temperatur og ligeså kunne bruges til at behandle forbrændinger og hjælpe rumkapsler til at mod
- Hvad er hastigheden og acceleraionen af en klippe, når den kastes op?
- Orkanrekorder slået i 2017
- Er lugten af eddike en kemisk egenskab?
- 3 klassifikationer af teknologi og giver eksempler for hver typer teknologi?
- Energi:Det er ikke kun for levende ting - en fysikforklaring
- Hvordan får luftmolekyler tættere på jorden deres varme?


