At tælle atomer og subatomære partikler i kemiske formler:en trin-for-trin guide
Af J.R. Kambak – Opdateret 30. august 2022
Hemera Technologies/PhotoObjects.net/Getty Images
En kemisk formel angiver de grundstoffer, der udgør en forbindelse, ved hjælp af symbolerne fra det periodiske system. Hvert symbol fortæller dig, hvilket grundstof der er til stede, og med et underskrift, hvor mange atomer af dette grundstof er i et enkelt molekyle. Subatomære partikler - protoner, neutroner og elektroner - udgør hvert atom. Atomvægten afspejler det samlede antal protoner og neutroner i kernen. Nedenfor gennemgår vi, hvordan man tæller både atomerne og de subatomære partikler for en typisk formel, ved at bruge calciumhydroxid, Ca(OH)₂, som et eksempel.
Tælle atomer i forbindelsen
Trin 1:Identificer elementerne
Læs formlen Ca(OH)₂ og find de forskellige grundstoffer:calcium (Ca), oxygen (O) og brint (H).
Trin 2:Bestem antallet af hvert atom
Se efter et underskrift efter hvert elementsymbol. Hvis ingen er til stede, er der ét atom af det element. I Ca(OH)₂ optræder calcium uden et underskrift, så der er ét Ca-atom.
Trin 3:Håndter polyatomiske ioner
Polyatomiske ioner er grupper af atomer, der fungerer som en enkelt enhed. De er sat i parentes. Tallet uden for parentesen angiver, hvor mange af den ion, der er til stede. Her er "OH" ionen, og underskriften 2 betyder, at der er to OH-grupper. Inde i ionen har oxygen og brint hver et implicit underskrift på 1. Multiplicer med 2:1 × 2 =2 atomer af O og 1 × 2 =2 atomer af H.
Sammenfatning:Ca – 1 atom; O – 2 atomer; H – 2 atomer.
Tælling af subatomære partikler i atomerne
Trin 1:Hent atomnumre og vægte
Brug en pålidelig kilde såsom IUPAC Periodic Table. Calcium (Ca) har et atomnummer på 20 og en atomvægt på 40,078. Oxygen (O) har 8 protoner/elektroner og en vægt på 15.999. Brint (H) har 1 proton/elektron og en vægt på 1,008.
Trin 2:Beregn protoner og elektroner
Atomnummeret er lig med antallet af protoner, og for et neutralt atom er antallet af elektroner det samme. Ca har således 20 protoner og 20 elektroner; O har 8 protoner og 8 elektroner; H har 1 proton og 1 elektron.
Trin 3:Bestem neutroner
Neutroner findes ved at trække atomnummeret fra massetallet (den afrundede atomvægt). For Ca er 40 – 20 =20 neutroner. For O, 16 – 8 =8 neutroner. Brint har ingen neutroner i sin mest almindelige isotop.
Trin 4:Sum partiklerne i Ca(OH)₂
Kombiner tællingerne fra de enkelte atomer:
- Protoner:20 (Ca) + 16 (2 × O) + 2 (2 × H) =38
- Elektroner:20 (Ca) + 16 (2 × O) + 2 (2 × H) =38
- Neutroner:20 (Ca) + 16 (2 × O) + 0 (2 × H) =36
Ting, du skal bruge
- Plideligt periodisk system (f.eks. IUPAC)
- Pen eller blyant
- Papir
- Lommeregner (til hurtig aritmetik)
 Varme artikler
Varme artikler
-
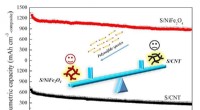 Nikkelferrit fremmer lithium-svovlbatteriets kapacitet og cyklusstabilitetSammenlignet med S/CNTer, S/NiFe2O4 har højere volumetrisk kapacitet og cykelstabilitet. Kredit:©Science China Press Lithium-svovl (Li-S) batteri kan blive praktisk, hvis 20 procent af de teoretis
Nikkelferrit fremmer lithium-svovlbatteriets kapacitet og cyklusstabilitetSammenlignet med S/CNTer, S/NiFe2O4 har højere volumetrisk kapacitet og cykelstabilitet. Kredit:©Science China Press Lithium-svovl (Li-S) batteri kan blive praktisk, hvis 20 procent af de teoretis -
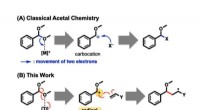 Radikal kemi muliggør ligetil syntese af ethereFigur 1. Aktiveringstilstand for acetaler. (A) Klassisk, acetal C-O-bindinger spaltes på heterolytisk vis. To elektroner, der udgør en C-O-binding, fjernes begge af en sur aktivator ([M]+) for at tilv
Radikal kemi muliggør ligetil syntese af ethereFigur 1. Aktiveringstilstand for acetaler. (A) Klassisk, acetal C-O-bindinger spaltes på heterolytisk vis. To elektroner, der udgør en C-O-binding, fjernes begge af en sur aktivator ([M]+) for at tilv -
 Forskere afslører en køreplan for at hjælpe med udvikling af osteoporosebehandlingFra venstre mod højre:forskningsassistent Ruben Garcia-Ordonez, Forskningsassistent Jie Zheng, Professor Pat Griffin, Forskningsassistent Scott Novick, Stabsforsker Mi Ra Chang. Kredit:Scripps Researc
Forskere afslører en køreplan for at hjælpe med udvikling af osteoporosebehandlingFra venstre mod højre:forskningsassistent Ruben Garcia-Ordonez, Forskningsassistent Jie Zheng, Professor Pat Griffin, Forskningsassistent Scott Novick, Stabsforsker Mi Ra Chang. Kredit:Scripps Researc -
 Forskere syntetiserer et nyt stof med antitumorale egenskaberLaboratoriet til syntese af naturlige produkter, hvor arbejdet er udført. Kredit:FEFUs pressekontor Forskere fra Far Eastern Federal University har udviklet et nyt syntetisk derivat af fascaplysin
Forskere syntetiserer et nyt stof med antitumorale egenskaberLaboratoriet til syntese af naturlige produkter, hvor arbejdet er udført. Kredit:FEFUs pressekontor Forskere fra Far Eastern Federal University har udviklet et nyt syntetisk derivat af fascaplysin
- Intel, Vivo senest til at droppe af tech show på grund af virus frygt
- Frit diffuserende cellulære proteiner når forkanten hurtigere
- NASA bestiller yderligere astronaut -taxiflyvninger fra Boeing og SpaceX til ISS
- Hvilken slags energi rejser til en brødrister?
- Holder det virkelig at tappe din dåse øl fra at bruse over dig?
- Hvad er de forskellige typer halvø?


