Forstå pH-ændringer ved fortynding af stærke syrer
Forståelse af pH og stærke syrer
* pH: Et mål for hydrogenionkoncentrationen ([H+]) i en opløsning. Lavere pH-værdier indikerer højere [H+], hvilket betyder en mere sur opløsning.
* Stærke syrer: Syrer, der fuldstændig ioniserer (dissocierer) i opløsning og frigiver alle deres hydrogenioner (H+). Eksempler:HCl (saltsyre), HNO3 (salpetersyre), H2SO4 (svovlsyre).
Fortynding og pH-ændring
1. Reduceret [H+] koncentration: Når du fortynder en stærk syre, tilsætter du mere opløsningsmiddel (normalt vand) til opløsningen. Dette reducerer koncentrationen af H+ ioner pr. volumenhed.
2. Skift i ligevægt: Mens stærke syrer ioniserer fuldstændigt, ændrer fortyndingen ikke det faktum, at syren stadig er til stede. Den reducerede [H+]-koncentration forskyder dog ligevægten en smule, hvilket gør ioniseringen af syren endnu mere fuldstændig.
3. pH-stigning: Da pH er omvendt proportional med [H+], resulterer et fald i [H+] i en stigning i pH.
Eksempel:
Forestil dig, at du har en opløsning af 1 M HCl (en stærk syre). Det ioniserer fuldstændigt og danner 1 M H+ og 1 M Cl-.
Hvis du fortynder denne opløsning med en faktor 10, bliver [H+] 0,1 M. Denne lavere koncentration fører til en højere pH (en mindre sur opløsning).
Nøglepunkt: Selvom fortyndingen af en stærk syre øger dens pH, er det vigtigt at huske, at selv fortyndede stærke syrer stadig er meget sure. pH-stigningen kan skifte opløsningen fra for eksempel pH 1 til pH 2, men den er stadig ret sur sammenlignet med en neutral opløsning (pH 7).
Sidste artikelpH-ændringer under syrefortynding:Forstå processen
Næste artikelForståelse af fortyndet saltsyre:sure egenskaber forklaret
 Varme artikler
Varme artikler
-
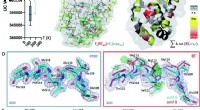 Sammenligning af kryogene strukturer med stuetemperaturprøver kan hjælpe med at identificere fejl …Fig. 1 Globale og lokale strukturelle reaktioner på temperatur. (A) Globalt, strukturer ved kryogene temperaturer (cryo; blå plot) er mere variable og mere kompakte end deres stuetemperatur (RT; røde
Sammenligning af kryogene strukturer med stuetemperaturprøver kan hjælpe med at identificere fejl …Fig. 1 Globale og lokale strukturelle reaktioner på temperatur. (A) Globalt, strukturer ved kryogene temperaturer (cryo; blå plot) er mere variable og mere kompakte end deres stuetemperatur (RT; røde -
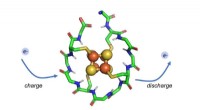 Forskere identificerer protein, der kan have eksisteret, da livet begyndteForskere har designet et syntetisk lille protein, der ombrydes omkring en metalkerne sammensat af jern og svovl. Dette protein kan gentagne gange oplades og udledes, gør det muligt for den at transpor
Forskere identificerer protein, der kan have eksisteret, da livet begyndteForskere har designet et syntetisk lille protein, der ombrydes omkring en metalkerne sammensat af jern og svovl. Dette protein kan gentagne gange oplades og udledes, gør det muligt for den at transpor -
 Træbaserede fibre opfanger hormoner fra spildevandOverfladen af garnet er belagt med et cyklisk sukker, der fanger forbindelserne ind i fiberens hulrum, når det svulmer i vand. Kredit:VTT VTT og Aalto University har udviklet et træbaseret cellu
Træbaserede fibre opfanger hormoner fra spildevandOverfladen af garnet er belagt med et cyklisk sukker, der fanger forbindelserne ind i fiberens hulrum, når det svulmer i vand. Kredit:VTT VTT og Aalto University har udviklet et træbaseret cellu -
 Sådan måler du luftfugtighed uden et hygrometer - en praktisk gør-det-selv-vejledningAf Megan Shoop Opdateret 24. marts 2022 Fugtighed er mængden af vanddamp i luften. Mens et hygrometer giver den mest præcise aflæsning, har mange mennesker ikke et derhjemme. Heldigvis har meteorolog
Sådan måler du luftfugtighed uden et hygrometer - en praktisk gør-det-selv-vejledningAf Megan Shoop Opdateret 24. marts 2022 Fugtighed er mængden af vanddamp i luften. Mens et hygrometer giver den mest præcise aflæsning, har mange mennesker ikke et derhjemme. Heldigvis har meteorolog
- Hvilken proces bruges til at bevæge sukkermolekyler over en cellemembran?
- Hvad er der i horisonten i 2022 efter et stort år for kryptovalutaer?
- At få fat i sagen:Overvågning i realtid af atom-mikroskopprober justerer for slid
- Hvilke fysiske egenskaber ved kobbertråd er uafhængige beløbet?
- Ptolemy Modified Model of the Universe at inkludere?
- Er den ekpyrotiske teori a af big bang?


