pH-ændringer under syrefortynding:Forstå processen
* pH og surhed: pH er et mål for koncentrationen af hydrogenioner (H+) i en opløsning. En lavere pH indikerer en højere H+ koncentration, hvilket gør opløsningen mere sur.
* Fortynding: Fortynding involverer tilsætning af mere opløsningsmiddel (vand i dette tilfælde) til en opløsning. Dette mindsker koncentrationen af det opløste stof (syre) i opløsningen.
* Reduceret koncentration af H+: Da syren nu er spredt ud over et større volumen, falder koncentrationen af H+ ioner.
* pH-stigning: Efterhånden som H+-koncentrationen falder, stiger pH-værdien og bevæger sig mod en mere neutral værdi (7).
Eksempel:
Forestil dig, at du har en stærk syre som saltsyre (HCl) i en koncentreret opløsning. Denne opløsning vil have en lav pH (f.eks. 1). Hvis du fortynder denne opløsning med vand, falder koncentrationen af HCl, og følgelig falder koncentrationen af H+ ioner. Dette resulterer i en højere pH (f.eks. 3).
Vigtig bemærkning: Mens fortynding generelt øger pH, er det vigtigt at huske, at stærke syrer forbliver stærke syrer selv efter fortynding. De vil stadig have et betydeligt antal H+ ioner, selvom pH er højere.
Sidste artikelFortynding og pH:Hvordan sur pH ændres, når den fortyndes
Næste artikelForstå pH-ændringer ved fortynding af stærke syrer
 Varme artikler
Varme artikler
-
 Krympefilm får grebKredit:American Chemical Society Mange mennesker husker med glæde at lege med legetøj kendt som Shrinky Dinks - plader af polystyrenplast med former, som børn kan farve, skær ud og varm i en ovn,
Krympefilm får grebKredit:American Chemical Society Mange mennesker husker med glæde at lege med legetøj kendt som Shrinky Dinks - plader af polystyrenplast med former, som børn kan farve, skær ud og varm i en ovn, -
 Havmuslinger er en model til forbedring af styrke, strækbarhed og vedhæftning i hydrogeler til så…Kredit:Pixabay/CC0 Public Domain Hydrogeler er overalt. De er vandelskende polymerer, der kan absorbere og tilbageholde vand, og kan findes i sådanne dagligdags forbrugerprodukter som bløde kontak
Havmuslinger er en model til forbedring af styrke, strækbarhed og vedhæftning i hydrogeler til så…Kredit:Pixabay/CC0 Public Domain Hydrogeler er overalt. De er vandelskende polymerer, der kan absorbere og tilbageholde vand, og kan findes i sådanne dagligdags forbrugerprodukter som bløde kontak -
 Beregningsstrategier overvinder hindringer i udviklingen af peptidterapiEn kunstners opfattelse af kraften ved beregningsmæssigt design til at udforske og belyse strukturerede peptider på tværs af det enorme energilandskab. Kredit:Vikram Mulligan/University of Washington
Beregningsstrategier overvinder hindringer i udviklingen af peptidterapiEn kunstners opfattelse af kraften ved beregningsmæssigt design til at udforske og belyse strukturerede peptider på tværs af det enorme energilandskab. Kredit:Vikram Mulligan/University of Washington -
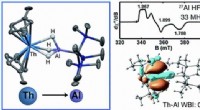 Thorium-aluminium-kompleks det første med et aktinid-element til at donere elektroner, når det bin…Kemisk Videnskab (2018). DOI:10.1039/C8SC01260A Et lille team af forskere fra University of California, Lawrence Berkeley National Laboratory og LPCNO, Université de Toulouse, har udviklet en måd
Thorium-aluminium-kompleks det første med et aktinid-element til at donere elektroner, når det bin…Kemisk Videnskab (2018). DOI:10.1039/C8SC01260A Et lille team af forskere fra University of California, Lawrence Berkeley National Laboratory og LPCNO, Université de Toulouse, har udviklet en måd
- Tyngdekraft her har mindre end halvdelen af trækket udøvet af på jorden?
- At forstå, hvad der får fangede gorillahjerter til at tikke
- Strukturel undersøgelse giver indsigt i, hvordan planter holder deres 'mund' lukket
- Uafhængige og afhængige er typer af dette inden for videnskab?
- Patent for arrays af elektriske prober i nanoskala tildelt NJIT i dag
- Tordenstorm, østlig vind:Hvordan skovbrandene blev så slemme


