Forståelse af væsker:egenskaber, definition og karakteristika
Fakta om væsker:
Definition og egenskaber:
* Bestemt volumen, ubestemt form: Væsker tager form af deres beholder, men opretholder et konstant volumen.
* Væske: Væsker kan flyde og ændre form under tryk.
* Høj tæthed: Generelt er væsker tættere end gasser, men mindre tætte end faste stoffer.
* Kompressibilitet: Væsker er mindre komprimerbare end gasser, men mere komprimerbare end faste stoffer.
* Viskositet: Væsker modstår strømning på grund af intern friktion. Jo højere viskositet, jo tykkere væske.
* Overfladespænding: Væsker udviser overfladespænding på grund af kohæsionskræfterne mellem molekyler, hvilket skaber en "hud" på overfladen.
Eksempler og applikationer:
* Vand: Den mest almindelige væske, afgørende for liv og mange industrielle processer.
* Olie: Anvendes til brændstof, smøring og madlavning.
* Kviksølv: Et flydende metal, der bruges i termometre og barometre.
* Blod: En livsvigtig væske i menneskekroppen.
* Alkohol: Anvendes i drikkevarer, medicin og som opløsningsmiddel.
* Væsker bruges i:
* Hydrauliske systemer: Generering af kraft ved hjælp af tryk.
* Kølesystemer: Overførsel af varme væk fra maskiner.
* Transport: Som brændstof, smøremidler og kølemidler.
* Mad- og drikkevareproduktion: Som ingredienser, opløsningsmidler og rengøringsmidler.
Interessante fakta:
* Vand udvider sig, når det fryser. Det er derfor isen flyder.
* Væsker kan fordampe. Dette er den proces, hvor en væske ændres til en gas.
* Væsker kan blandes. Nogle væsker blandes let, mens andre ikke gør det.
* Nogle væsker kan underkøles. Det betyder, at de kan afkøles til under frysepunktet uden at fryse.
* Lydens hastighed er hurtigere i væsker end i gasser.
Bonus:
* Væsker er en af stoffets tre tilstande sammen med faste stoffer og gasser.
* Undersøgelsen af væsker kaldes væskedynamik.
Dette er blot et indblik i væskernes verden. Der er meget mere at lære om disse fascinerende stoffer.
Sidste artikelpH 5-6 Væsker:Almindelige eksempler og deres surhedsgrad
Næste artikelIltsammensætning:Forstå fraværet af nitrogen
 Varme artikler
Varme artikler
-
 Gennemsigtig gennem mad og stofforfalskninger og bedragerierEn ny metode identificerer stoffer ved at undersøge, hvordan de ændrer sig efter at være nedsænket i flydende nitrogen. Kredit:American Chemical Society Hvis vi kunne fortælle autentisk fra forfal
Gennemsigtig gennem mad og stofforfalskninger og bedragerierEn ny metode identificerer stoffer ved at undersøge, hvordan de ændrer sig efter at være nedsænket i flydende nitrogen. Kredit:American Chemical Society Hvis vi kunne fortælle autentisk fra forfal -
 Forskere udvikler smartphone-læser til hurtigere infektionstestWSU-professor Lei Li og kandidatstuderende Yu-Chung Chang (l-r) tester den nye smartphone, der opdager 12 almindelige virale og bakterielle infektionssygdomme. Kredit:Washington State University W
Forskere udvikler smartphone-læser til hurtigere infektionstestWSU-professor Lei Li og kandidatstuderende Yu-Chung Chang (l-r) tester den nye smartphone, der opdager 12 almindelige virale og bakterielle infektionssygdomme. Kredit:Washington State University W -
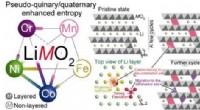 Forskere frigør potentielle midler til at reducere afhængigheden af sjældne metallerGrafisk abstrakt. Kredit:ACS Applied Energy Materials (2022). DOI:10.1021/acsaem.1c03968 En forskergruppe, der bruger billige elementer, har demonstreret gennemførligheden af at syntetisere elekt
Forskere frigør potentielle midler til at reducere afhængigheden af sjældne metallerGrafisk abstrakt. Kredit:ACS Applied Energy Materials (2022). DOI:10.1021/acsaem.1c03968 En forskergruppe, der bruger billige elementer, har demonstreret gennemførligheden af at syntetisere elekt -
 Opdag, hvad der får durian til at stinkeBillede af en durian. Kredit:Martin Steinhaus Forskere ved Leibniz-Institut for Food Systems Biology ved det tekniske universitet i München (Leibniz-LSB@TUM) har bekræftet tilstedeværelsen af de
Opdag, hvad der får durian til at stinkeBillede af en durian. Kredit:Martin Steinhaus Forskere ved Leibniz-Institut for Food Systems Biology ved det tekniske universitet i München (Leibniz-LSB@TUM) har bekræftet tilstedeværelsen af de
- Undersøgelse:Befolkninger af vidt udbredte træarter reagerer forskelligt på klimaændringer
- Hvor lang tid tog det for planeterne at danne?
- Hvilke tre ting kan ske, når varmeenergi overføres til stof ved stråling?
- Smeltende is og en udgravning i høj højde afslører vikingehemmeligheder i Norge
- Hvorfor måler videnskabsmand, hvor hurtig vind blæser?
- Hvilken stat gjorde et kæmpe meteorland?


