Sølvioner og ioniske bindinger:Forstå forskellen
Her er hvorfor:
* ioniske bindinger er de elektrostatiske tiltrækningskræfter mellem modsat ladede ioner. De forekommer *mellem* to eller flere atomer.
* Sølvioner er enkelte, ladede arter. De dannes, når et sølvatom mister en elektron.
Tænk på det på denne måde:
* En ionbinding er som et ægteskab mellem to ioner.
* En sølvion er som en enkelt person, klar til at blive gift (danne et ionbånd) med en passende partner.
Eksempler på ionbindinger:
* Natriumchlorid (NaCl):Natriumioner (Na+) og chloridioner (Cl-) holdes sammen af en ionbinding.
* Calciumoxid (CaO):Calciumioner (Ca2+) og oxidioner (O2-) holdes sammen af en ionbinding.
Sølvioner kan deltage i ionbindinger. For eksempel kan de danne en ionbinding med en chloridion for at skabe sølvchlorid (AgCl). Men selve sølvionen er ikke bindingen; det er en af deltagerne i obligationen.
 Varme artikler
Varme artikler
-
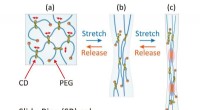 Biokompatible hydrogelmaterialer kan hurtigt komme sig efter mekanisk belastningEn strain gauge trækker prøver af hydrogel fra hinanden. (Øvre) En typisk gel med et hak skåret i venstre side snappede kort tid efter at den var strakt. (Midt) Den nye selvforstærkede gel havde et ha
Biokompatible hydrogelmaterialer kan hurtigt komme sig efter mekanisk belastningEn strain gauge trækker prøver af hydrogel fra hinanden. (Øvre) En typisk gel med et hak skåret i venstre side snappede kort tid efter at den var strakt. (Midt) Den nye selvforstærkede gel havde et ha -
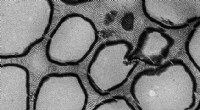 Efterligner en sød løsning til at fjerne forureningEt transmissionselektronmikroskopi (TEM) billede viser, at de sfæriske rum er forbundet gennem nanokanaler. Kredit:S. Nunes En hurtig, sikker metode til at fremstille et 3-D porøst materiale, der
Efterligner en sød løsning til at fjerne forureningEt transmissionselektronmikroskopi (TEM) billede viser, at de sfæriske rum er forbundet gennem nanokanaler. Kredit:S. Nunes En hurtig, sikker metode til at fremstille et 3-D porøst materiale, der -
 Forskere udvikler en ny måde at fjerne forurenende stoffer fra vand påForskere har udviklet en ny metode til at fjerne selv ekstremt lave niveauer af uønskede forbindelser fra vand. Den nye metode er afhængig af en elektrokemisk proces til selektivt at fjerne organiske
Forskere udvikler en ny måde at fjerne forurenende stoffer fra vand påForskere har udviklet en ny metode til at fjerne selv ekstremt lave niveauer af uønskede forbindelser fra vand. Den nye metode er afhængig af en elektrokemisk proces til selektivt at fjerne organiske -
 High-throughput platform muliggør aktivitetskortlægning af nye kræftlægemålEn lysin -methyltransferase fastgjort til et substrat. Den tændte del viser en methylgruppe, der tilsættes af methyltransferasen. Kredit:Dr. Bradley Dickson/Rothbart Laboratory ved Van Andel Research
High-throughput platform muliggør aktivitetskortlægning af nye kræftlægemålEn lysin -methyltransferase fastgjort til et substrat. Den tændte del viser en methylgruppe, der tilsættes af methyltransferasen. Kredit:Dr. Bradley Dickson/Rothbart Laboratory ved Van Andel Research
- Ingeniører udvikler ultratynde, ultralet nanokort
- GPM-satellit fund afklippet Orkanen Jose har meget høje storme
- Europæisk, Canadiske tilsynsmyndigheder skal lave deres egen gennemgang af Boeing-jetfly
- As The Crust Turns:Cassini Data Show Enceladus in Motion
- Hvilke elementer kan opdeles i nogen enklere stoffer?
- Hvor meget tyngdekraft er der i en stjerne?


