Aluminium og kobbersulfatreaktion:Kemisk ligning og forklaring
Her er den afbalancerede kemiske ligning:
2 Al + 3 CuSO4 → Al2(SO4)3 + 3 Cu
Forklaring:
* Aluminium er mere reaktivt end kobber. Dette betyder, at det kan fortrænge kobber fra sin forbindelse.
* Aluminiumsatomer mister elektroner (oxidation) og bliver til aluminiumioner (Al³⁺).
* Kobberioner (Cu²⁺) i kobbersulfatopløsningen får elektroner (reduktion) og bliver til kobberatomer.
* Sulfationerne (SO₄²⁻) forbliver uændrede og kombineres med aluminiumionerne for at danne aluminiumsulfat.
Observation:
* Når du blander aluminium og kobbersulfatopløsning, vil du se en rødbrun belægning af kobbermetal dannes på overfladen af aluminium.
* Opløsningen vil ændre farve fra blå (på grund af CuSO₄) til farveløs (på grund af Al₂(SO₄)3).
* Reaktionen er eksoterm, hvilket betyder, at den frigiver varme, og opløsningen kan blive let varm.
Bemærk: Denne reaktion er en god demonstration af reaktivitetsrækken af metaller. Aluminium er højere i reaktivitetsserien end kobber, så det kan fortrænge kobber fra dets forbindelse.
Sidste artikelHalogener:Forståelse af grundstofferne F, Cl, Br, I, At
Næste artikelSølvioner og ioniske bindinger:Forstå forskellen
 Varme artikler
Varme artikler
-
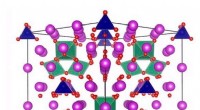 Finjustering af kemi ved doping med overgangsmetaller gav stabilitet i bismuthoxidKredit:Australian Nuclear Science and Technology Organisation (ANSTO) ANSTO har bidraget til forskning ledet af University of Sydney, involverer doping af overgangsmetaller i en polymorf af bismut
Finjustering af kemi ved doping med overgangsmetaller gav stabilitet i bismuthoxidKredit:Australian Nuclear Science and Technology Organisation (ANSTO) ANSTO har bidraget til forskning ledet af University of Sydney, involverer doping af overgangsmetaller i en polymorf af bismut -
 Fremstilling af aluminiumslegering nu 50 % mere energieffektivBilleder af aluminiumslegering 7075 taget med et scanningselektronmikroskop før (A), under (B) og efter (C) gennemgang af ShaPE-maskinen viser, hvordan legeringens mikrostruktur ændrer sig dramatisk u
Fremstilling af aluminiumslegering nu 50 % mere energieffektivBilleder af aluminiumslegering 7075 taget med et scanningselektronmikroskop før (A), under (B) og efter (C) gennemgang af ShaPE-maskinen viser, hvordan legeringens mikrostruktur ændrer sig dramatisk u -
 Elementer, der forbliver gasformige eller flydende ved standardtryk:Frysepunkter under 0°CThinkstock Images/Stockbyte/Getty Images Et stofs tilstand – om det er en gas, væske eller fast stof – afhænger af både tryk og temperatur. For at standardisere sammenligninger bruger forskere et sæt
Elementer, der forbliver gasformige eller flydende ved standardtryk:Frysepunkter under 0°CThinkstock Images/Stockbyte/Getty Images Et stofs tilstand – om det er en gas, væske eller fast stof – afhænger af både tryk og temperatur. For at standardisere sammenligninger bruger forskere et sæt -
 Mellemlag hjælper perovskitkrystallisering til højtydende lysemitterende dioderForskellige metaloxidlag påvirker egenskaberne af de tynde perovskitfilm. Kredit:Charlotte Perhammar Forskere ved LiU, der arbejder med kolleger fra Kina, har vist, hvordan man opnår effektive per
Mellemlag hjælper perovskitkrystallisering til højtydende lysemitterende dioderForskellige metaloxidlag påvirker egenskaberne af de tynde perovskitfilm. Kredit:Charlotte Perhammar Forskere ved LiU, der arbejder med kolleger fra Kina, har vist, hvordan man opnår effektive per
- Hvordan påvirker magneter under termometre dens evne til at fortælle temperaturen?
- I begyndelsen af det syttende århundrede spanske kontrollerede territorium, hvorpå kontinenter?
- Eliminering af eksponenter i algebraiske ligninger:En praktisk vejledning
- Viser sammenfiltring gennem et fiberkabel med høj kvalitet
- Jægernes måne vil gløde i top, orange herlighed denne weekend
- Ricin er kun dødelig i kombination med sukker


