Van der Waals Forces:Understanding Molecular Attraction
Der er tre typer van der Waals-kræfter:
* Spredningskræfter i London: Disse er den svageste type og forekommer mellem alle molekyler, selv ikke-polære. De opstår som følge af midlertidige udsving i elektronfordelingen omkring molekylet.
* Dipol-dipolkræfter: Disse forekommer mellem polære molekyler, der har permanente dipoler på grund af ujævn deling af elektroner.
* Hydrogenbinding: Dette er den stærkeste type van der Waals-kraft og opstår, når et brintatom er bundet til et meget elektronegativt atom (som oxygen, nitrogen eller fluor).
Disse kræfter er relativt svage sammenlignet med ioniske eller kovalente bindinger, men de er stadig vigtige ved bestemmelse af stoffers fysiske egenskaber, såsom smeltepunkt, kogepunkt og opløselighed.
 Varme artikler
Varme artikler
-
 Opdagelse rejser muligheden for at behandle neurologiske lidelserKredit:University of Dundee Opdagelsen af en ny klasse af enzymer i human biologi af forskere ved University of Dundee har åbnet et nyt forskningsområde, der kan gavne patienter, der lider af en
Opdagelse rejser muligheden for at behandle neurologiske lidelserKredit:University of Dundee Opdagelsen af en ny klasse af enzymer i human biologi af forskere ved University of Dundee har åbnet et nyt forskningsområde, der kan gavne patienter, der lider af en -
 Tidlig advarselssensor opsnuser skadelig gas i byerKredit: ACS sensorer (2020). DOI:10.1021/acssensors.9b02318 En integreret detektorenhed kunne danne grundlag for et distribueret luftkvalitetssensornetværk. Designet til en elektronisk sensor, d
Tidlig advarselssensor opsnuser skadelig gas i byerKredit: ACS sensorer (2020). DOI:10.1021/acssensors.9b02318 En integreret detektorenhed kunne danne grundlag for et distribueret luftkvalitetssensornetværk. Designet til en elektronisk sensor, d -
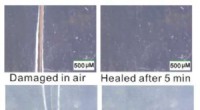 Forskere opdager ny type selvhelbredende materialeØverste panel:Optiske mikroskopbilleder af beskadigede (venstre) og reparerede (højre) prøver af et af materialerne i luft ved 25 °C. En film blev knækket af et barberblad og derefter efterladt i luft
Forskere opdager ny type selvhelbredende materialeØverste panel:Optiske mikroskopbilleder af beskadigede (venstre) og reparerede (højre) prøver af et af materialerne i luft ved 25 °C. En film blev knækket af et barberblad og derefter efterladt i luft -
 Spiropyran-funktionaliserede fotokromiske nylonbånd til langtidsføling af ultraviolet lys(a) Snapshots af SP-funktionaliserede webbings over otte ugers UV-eksponering. (b) Tidsmæssig udvikling af webbingsets farve repræsenteret i CIE 1976-farverummet. Indsatsen er en zoomet visning, og de
Spiropyran-funktionaliserede fotokromiske nylonbånd til langtidsføling af ultraviolet lys(a) Snapshots af SP-funktionaliserede webbings over otte ugers UV-eksponering. (b) Tidsmæssig udvikling af webbingsets farve repræsenteret i CIE 1976-farverummet. Indsatsen er en zoomet visning, og de
- Nye spor om et uhåndgribeligt materiale:En superleder, der kan syntetiseres i laboratoriet
- Hvad er den termiske energioverførsel, der opstår ved bevægelse af væske i væske eller gas?
- Hvad er et eksempel på ferromagnetisk materiale?
- Er smeltning og kogepunkt fysiske egenskaber ved et stof?
- Sådan bruger du en times table (det er ikke magi, det er huske)
- En metode med rødder i AI afdækker, hvordan mennesker træffer valg, grupper og sociale medier


