Ammoniak- og zinkchloridreaktion:afbalanceret ligning og forklaring
Her er den afbalancerede ligning for denne reaktion:
ZnCl2 (aq) + 4 NH3 (aq) ⇌ [Zn(NH3) 4]²+ (aq) + 2 Cl⁻ (aq)
Forklaring:
* ZnCl2 (vandig): Zinkchlorid opløses i vand og danner vandige ioner.
* NH3 (vandig): Ammoniak opløses også i vand og danner vandige ammoniakmolekyler.
* [Zn(NH₃)₄]²⁺ (vandig): Dette er tetraamminezinc(II)-ionen, en kompleks ion, der dannes, når fire ammoniakmolekyler koordinerer til en zink(II)-ion.
* Cl⁻ (vandig): Chloridioner frigives fra zinkchloridet.
Vigtige bemærkninger:
* Reaktionen er reversibel, hvilket betyder, at den kan fortsætte i begge retninger. Ligevægten favoriserer dannelsen af den komplekse ion.
* Reaktionen er en Lewis syre-base reaktion. Zinkchlorid fungerer som en Lewis-syre, der accepterer elektronpar fra ammoniak, der fungerer som en Lewis-base.
Sig til, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
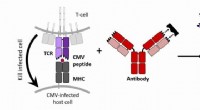 Udstyrelse af T -celleceptorer til bekæmpelse af en udbredt og undertiden dødelig virusT-celler er dygtige til at dræbe cytomegalovirus (CMV)-inficerede celler i kraft af en T-cellereceptor (TCR), der genkender intracellulære CMV-associerede proteiner, der bliver præsenteret på celleove
Udstyrelse af T -celleceptorer til bekæmpelse af en udbredt og undertiden dødelig virusT-celler er dygtige til at dræbe cytomegalovirus (CMV)-inficerede celler i kraft af en T-cellereceptor (TCR), der genkender intracellulære CMV-associerede proteiner, der bliver præsenteret på celleove -
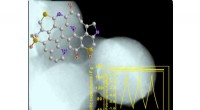 Højt nitrogen og svovl dobbelt-dopede kulstofmikrosfærer til superkondensatorerDenne figur viser morfologien, molekylær model og cyklisk ydeevne af den N/S co-doterede kulstofmikrosfære. Kredit:©Science China Press Blandt elektrodematerialer til superkondensatorer, kulstofba
Højt nitrogen og svovl dobbelt-dopede kulstofmikrosfærer til superkondensatorerDenne figur viser morfologien, molekylær model og cyklisk ydeevne af den N/S co-doterede kulstofmikrosfære. Kredit:©Science China Press Blandt elektrodematerialer til superkondensatorer, kulstofba -
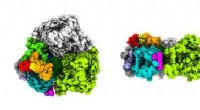 Unikke pigmenter i fotosyntetiske marinebakterier afslører, hvordan den lever i svagt lysFigur 1:Et kryo-elektronmikroskopi tæthedskort over Acaryochloris marina fotosystem I afslører strukturelle elementer, der gør det muligt for det at omdanne lavenergilys til kemisk energi. Kredit:Æn
Unikke pigmenter i fotosyntetiske marinebakterier afslører, hvordan den lever i svagt lysFigur 1:Et kryo-elektronmikroskopi tæthedskort over Acaryochloris marina fotosystem I afslører strukturelle elementer, der gør det muligt for det at omdanne lavenergilys til kemisk energi. Kredit:Æn -
 Cement, salt og vand:Et nyt lagermateriale til grøn varmeKredit:CC0 Public Domain Opvarmning af det rum, hvor vi bor eller arbejder, er en almindelig nødvendighed i de fleste beboede områder. Den energi, der kræves til denne proces, er ansvarlig for en
Cement, salt og vand:Et nyt lagermateriale til grøn varmeKredit:CC0 Public Domain Opvarmning af det rum, hvor vi bor eller arbejder, er en almindelig nødvendighed i de fleste beboede områder. Den energi, der kræves til denne proces, er ansvarlig for en
- Video:Aeolus timelapse
- Stigende CO2 forårsager mere end en klimakrise – det kan direkte skade vores evne til at tænke
- Sydney indfører første vandrestriktioner i årti
- Hvad er nogle fælles husholdningssyrer og baser?
- Hvordan er den kontinentale drift relateret til pladetektonik?
- Hvad er enheder, der bruger halvledere til at producere elektricitet fra solenergi?


