Kovalente bindinger:Forståelse af elektrondeling og molekylær stabilitet
* Atomer søger stabilitet: Atomer er mest stabile, når deres ydre elektronskal (valensskal) er fuld. Dette betyder normalt at have 8 elektroner (oktetreglen).
* Deling af elektroner: Atomer med ufuldstændige ydre skaller kan opnå stabilitet ved at dele elektroner med andre atomer.
* Kovalent bindingsdannelse: Dette fælles elektronpar danner en kovalent binding, der holder de to atomer sammen.
* Stabilitet og molekyledannelse: De delte elektroner tiltrækkes af begge kerner, hvilket skaber en stærk elektrostatisk kraft, der holder atomerne i et fast arrangement og danner et molekyle.
Eksempel:
* Et brintatom (H) har en elektron i sin ydre skal og har brug for en mere for at være stabil.
* To brintatomer kan dele deres enkelte elektroner og danne en kovalent binding og danne et brintmolekyle (H₂).
Nøglepunkter:
* Kovalente bindinger er generelt stærkere end ionbindinger.
* Kovalente bindinger kan være enkelt-, dobbelt- eller tredobbelte, afhængigt af antallet af delte elektroner.
* Kovalent binding er ansvarlig for dannelsen af en bred vifte af molekyler, fra simple molekyler som vand (H2O) til komplekse biologiske molekyler som DNA.
 Varme artikler
Varme artikler
-
 Forskere udvikler en ny enhed til at opdage gluten mere effektivtKredit:Asociacion RUVID Tæt på 1 procent af verdens befolkning lider af cøliaki, en kompleks og autoimmun lidelse forårsaget af indtagelse af gluten, og for hvilken der ikke er nogen behandling ud
Forskere udvikler en ny enhed til at opdage gluten mere effektivtKredit:Asociacion RUVID Tæt på 1 procent af verdens befolkning lider af cøliaki, en kompleks og autoimmun lidelse forårsaget af indtagelse af gluten, og for hvilken der ikke er nogen behandling ud -
 Forskere udvikler papirbaserede sensorer til kuldioxidDen papirbaserede sensor udviklet af U of A-forskere bliver orange, når den udsættes for kuldioxid. Forskerne siger, at det er billigt, sensorer, der er nemme at producere, kan bruges i smarte bygning
Forskere udvikler papirbaserede sensorer til kuldioxidDen papirbaserede sensor udviklet af U of A-forskere bliver orange, når den udsættes for kuldioxid. Forskerne siger, at det er billigt, sensorer, der er nemme at producere, kan bruges i smarte bygning -
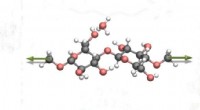 Konvertering af biomasse ved at anvende mekanisk kraftDen molekylære struktur af cellulose, som nanovidenskabsmænd påførte mekanisk kraft (grønne pile). Hydrolysereaktionen ændrede sig dramatisk som følge heraf. Kredit:Saeed Amirjalayer et al./Angew Chem
Konvertering af biomasse ved at anvende mekanisk kraftDen molekylære struktur af cellulose, som nanovidenskabsmænd påførte mekanisk kraft (grønne pile). Hydrolysereaktionen ændrede sig dramatisk som følge heraf. Kredit:Saeed Amirjalayer et al./Angew Chem -
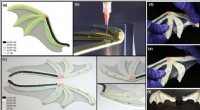 Forskere bryder ny vej inden for 3D-printet blød robotteknologi med det største udvalg af polymerh…(a) Illustration af det strukturelle design. (b) Direkte blæk-skrivning af hybridstrukturen. (c) Hærdet struktur (areal på ~90 cm 2 per vinge, membrantykkelse ~0,7 mm, total armtykkelse ~3,5 mm). (d
Forskere bryder ny vej inden for 3D-printet blød robotteknologi med det største udvalg af polymerh…(a) Illustration af det strukturelle design. (b) Direkte blæk-skrivning af hybridstrukturen. (c) Hærdet struktur (areal på ~90 cm 2 per vinge, membrantykkelse ~0,7 mm, total armtykkelse ~3,5 mm). (d


