Kaliumhydroxid og salpetersyreneutralisering:Ionisk ligning og forklaring
1. Komplet ionisk ligning:
* KOH(aq) → K⁺(aq) + OH⁻(vandig)
* HNO₃(aq) → H⁺(vandig) + NO₃⁻(vandig)
* K⁺(aq) + OH⁻(vandig) + H⁺(vandig) + NO₃⁻(vandig) → H2O(l) + K⁺(aq) + NO₃⁻(vandig)
2. Net-ionisk ligning:
* H⁺(vandig) + OH⁻(vandig) → H2O(l)
Forklaring:
* Fuldstændig ionisk ligning: Viser alle ioner til stede i opløsning før og efter reaktionen.
* Net-ionisk ligning: Fokuserer på de arter, der faktisk deltager i reaktionen. Tilskuerioner (K⁺ og NO3⁻) annulleres, fordi de forbliver uændrede under hele reaktionen.
Nøglepunkter:
* Neutralisering: Reaktionen af en syre og en base, der danner salt og vand.
* Ionisk ligning: Repræsenterer reaktionen med hensyn til dens bestanddele ioner.
* Tilskuerioner: Ioner, der ikke direkte deltager i reaktionen.
 Varme artikler
Varme artikler
-
 Forskere skaber lokkemaling, der lurer infrarøde kameraerBogstaverne C-A-L fremstår seje, selvom miljøet er varmt. UC Berkeley -ingeniører udvikler et lokkedue, der lader infrarøde kameraer til at opfatte en bestemt temperatur frem for objektets faktiske te
Forskere skaber lokkemaling, der lurer infrarøde kameraerBogstaverne C-A-L fremstår seje, selvom miljøet er varmt. UC Berkeley -ingeniører udvikler et lokkedue, der lader infrarøde kameraer til at opfatte en bestemt temperatur frem for objektets faktiske te -
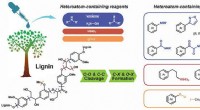 Varianter af funktionaliserede aromater ekspanderet ved heteroatom-deltaget lignin-spaltningHeteroatom-holdige reagenser udløser den katalytiske spaltning af ligninbindinger og funktionalisering af produkter samtidigt. Kredit:LI Hongji Lignin er det aromatiske polymerfragment af lignocel
Varianter af funktionaliserede aromater ekspanderet ved heteroatom-deltaget lignin-spaltningHeteroatom-holdige reagenser udløser den katalytiske spaltning af ligninbindinger og funktionalisering af produkter samtidigt. Kredit:LI Hongji Lignin er det aromatiske polymerfragment af lignocel -
 Neutroner gør strukturelle ændringer i molekylære børster synligeDr. Lester Barnsley, instrumentforsker ved Forschungszentrum Juelich, ved det lillevinklede neutronspredningssystem KWS-1 i Heinz Maier-Leibnitz Zentrum ved Heinz Maier-Leibnitz Research Neutron Sourc
Neutroner gør strukturelle ændringer i molekylære børster synligeDr. Lester Barnsley, instrumentforsker ved Forschungszentrum Juelich, ved det lillevinklede neutronspredningssystem KWS-1 i Heinz Maier-Leibnitz Zentrum ved Heinz Maier-Leibnitz Research Neutron Sourc -
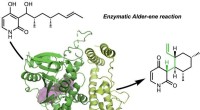 Forskere opdager de første enzymer til at katalysere en klassisk organisk reaktionKredit:University of California, Los Angeles The Tang, Garg, og Houk-forskningsgrupper har opdaget naturens naturlige proteinkatalysatorer (enzymer), der katalyserer Alder-en-reaktionen. Alle gru
Forskere opdager de første enzymer til at katalysere en klassisk organisk reaktionKredit:University of California, Los Angeles The Tang, Garg, og Houk-forskningsgrupper har opdaget naturens naturlige proteinkatalysatorer (enzymer), der katalyserer Alder-en-reaktionen. Alle gru


