Kovalente bindinger og elektrisk ledningsevne:Forstå forskellen
* Elektrondeling: I kovalente bindinger deles elektroner mellem atomer og danner en stærk binding. Disse elektroner er lokaliseret mellem atomerne og kan ikke bevæge sig frit gennem hele materialet.
* Ingen frie elektroner: I modsætning til metalliske bindinger, hvor elektroner er delokaliseret og kan bevæge sig frit, mangler kovalente bindinger frie elektroner til at føre elektrisk strøm.
Undtagelser:
Mens de fleste kovalente forbindelser er dårlige ledere, er der nogle få undtagelser:
* Grafit: Grafit er en god leder på grund af sin unikke struktur. Mens kulstofatomerne i hvert lag holdes sammen af stærke kovalente bindinger, holdes lagene sammen af svage van der Waals-kræfter. Dette tillader elektroner at bevæge sig frit mellem lagene, hvilket gør grafit til en god leder af elektricitet.
* Konduktive polymerer: Nogle polymerer med konjugerede systemer (alternerende enkelt- og dobbeltbindinger) kan udvise ledningsevne på grund af delokalisering af elektroner langs kæden.
Opsummering: Kovalente bindinger danner typisk materialer, der er dårlige ledere af elektricitet. Imidlertid kan specifikke strukturer, såsom grafit og nogle ledende polymerer, udvise ledningsevne.
 Varme artikler
Varme artikler
-
 Accelererende opdagelse af elektrokatalysatorEn webgrænseflade, der viser deres elektrokatalysator forudsigelser, bygget af en CMU-baseret computerklasse. Kredit:Zack Ulissi Forskere baner vejen for total afhængighed af vedvarende energi, da
Accelererende opdagelse af elektrokatalysatorEn webgrænseflade, der viser deres elektrokatalysator forudsigelser, bygget af en CMU-baseret computerklasse. Kredit:Zack Ulissi Forskere baner vejen for total afhængighed af vedvarende energi, da -
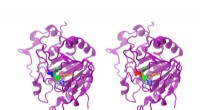 Simulering af AsqJ-enzymet åbner op for nye muligheder for farmaceutisk kemiMens forskellen mellem den naturlige og den modificerede AsqJ kun er én aminosyre, reaktiviteten er klart anderledes. Den naturlige AsqJ (venstre) har en valin i position 72 (blå). Den modificerede fo
Simulering af AsqJ-enzymet åbner op for nye muligheder for farmaceutisk kemiMens forskellen mellem den naturlige og den modificerede AsqJ kun er én aminosyre, reaktiviteten er klart anderledes. Den naturlige AsqJ (venstre) har en valin i position 72 (blå). Den modificerede fo -
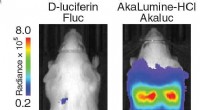 I levende farver:at se celler udefra kroppen med syntetisk bioluminescensBioluminescensbilleder af mus intravenøst injiceret med 103 HeLa-celler, der udtrykker Fluc (venstre) eller Akaluc (højre). Substratadministration blev udført intraperitonealt. Billeder blev erhverv
I levende farver:at se celler udefra kroppen med syntetisk bioluminescensBioluminescensbilleder af mus intravenøst injiceret med 103 HeLa-celler, der udtrykker Fluc (venstre) eller Akaluc (højre). Substratadministration blev udført intraperitonealt. Billeder blev erhverv -
 Elementer, der forbliver gasformige eller flydende ved standardtryk:Frysepunkter under 0°CThinkstock Images/Stockbyte/Getty Images Et stofs tilstand – om det er en gas, væske eller fast stof – afhænger af både tryk og temperatur. For at standardisere sammenligninger bruger forskere et sæt
Elementer, der forbliver gasformige eller flydende ved standardtryk:Frysepunkter under 0°CThinkstock Images/Stockbyte/Getty Images Et stofs tilstand – om det er en gas, væske eller fast stof – afhænger af både tryk og temperatur. For at standardisere sammenligninger bruger forskere et sæt
- Hvad amerikanere bør frygte i cyberspace
- Hvad er den kemiske ligning for 2naci?
- Hvorfor lyd rejser i forskellige hastighedsmaterialer?
- Hvilken planet rejser rundt om solen med laveste hastighed?
- Hvad forårsager de mørke bånd, der er observeret i et solspektrum?
- Hvad er stadierne i stjernelivet på et flowdiagram?


