Fluor vs. Brom:Elektronaffinitetssammenligning og -forklaring
* Mindre størrelse: Fluor er mindre end brom. Dette betyder, at den yderste elektron i fluor er tættere på kernen og oplever en stærkere tiltrækningskraft.
* Højere effektiv nuklear ladning: Fluor har en højere effektiv nuklear ladning (den positive ladning mærket af den yderste elektron) end brom. Dette skyldes den mindre størrelse og det stigende antal protoner i kernen, når du bevæger dig ned i halogengruppen.
Elektronaffinitet er ændringen i energi, når en elektron føjes til et neutralt atom i gasform. En mere negativ elektronaffinitet indikerer en større tendens til at få en elektron.
Derfor resulterer fluors mindre størrelse og højere effektive kerneladning i en mere negativ elektronaffinitet sammenlignet med brom.
 Varme artikler
Varme artikler
-
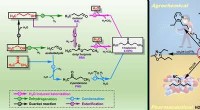 Forskere fremmer biomassetransformationsprocessen(A) Dette er en foreslået reaktionsvej, der fører til 4-HPO. (B) Dette er 4-HPO-udnyttelse. Kredit:DICP Biomasse kan tjene som en vedvarende kilde til både energi og kulstof. Acetone, n-butanol, o
Forskere fremmer biomassetransformationsprocessen(A) Dette er en foreslået reaktionsvej, der fører til 4-HPO. (B) Dette er 4-HPO-udnyttelse. Kredit:DICP Biomasse kan tjene som en vedvarende kilde til både energi og kulstof. Acetone, n-butanol, o -
 Coronavirus-testsæt skal udvikles ved hjælp af ny RNA-billeddannelsesteknologiSFU-forsker Lena Dolgosheina holder rør op for at demonstrere Mango-billedteknologien. Kredit:Simon Fraser University Simon Fraser University-forskere vil bruge deres banebrydende billedteknologi
Coronavirus-testsæt skal udvikles ved hjælp af ny RNA-billeddannelsesteknologiSFU-forsker Lena Dolgosheina holder rør op for at demonstrere Mango-billedteknologien. Kredit:Simon Fraser University Simon Fraser University-forskere vil bruge deres banebrydende billedteknologi -
 Forskere præsenterer ny strategi for at udvide duktiliteten i en enfaset legeringA. Multilevel heterogen struktur af enfaset CrCoNi medium entropi-legering efter træktest:korn på størrelse med mikrometer (hvide), submikronkorn (blå), nanokorn (farvede). Nanograin dannes ved korngr
Forskere præsenterer ny strategi for at udvide duktiliteten i en enfaset legeringA. Multilevel heterogen struktur af enfaset CrCoNi medium entropi-legering efter træktest:korn på størrelse med mikrometer (hvide), submikronkorn (blå), nanokorn (farvede). Nanograin dannes ved korngr -
 Forskningssamarbejde bringer nye koncepter for kalium-ion-batterierDette billede viser carbon nanofibre analyseret med en teknik kaldet energispredende røntgenspektroskopi efter at have gennemgået ladningsafladningscyklus i nye kaliumionbatterier. Batterierne er unde
Forskningssamarbejde bringer nye koncepter for kalium-ion-batterierDette billede viser carbon nanofibre analyseret med en teknik kaldet energispredende røntgenspektroskopi efter at have gennemgået ladningsafladningscyklus i nye kaliumionbatterier. Batterierne er unde
- Serverer en fåremælks smoothie
- Hvilken organelle frigiver kemikalier, der nedbryder og genanvender celler organeller?
- Ingeniører producerer et fisheye -objektiv, der er helt fladt
- Hvilken type kemiske reaktioner katalyserer kinaser?
- Hvad gør symboler?
- Hvilken energi er i form af vand, der er opbevaret i en tank ved bygningstak?


