Forståelse af fordampning:Hvordan væsker konverteres til gas
1. Varmeenergi: Nøglen er at tilføje varmeenergi til væsken. Denne energi får molekylerne i væsken til at bevæge sig hurtigere og længere fra hinanden.
2. Overvindelse af intermolekylære kræfter: Væsker holdes sammen af svage intermolekylære kræfter (som brintbindinger, van der Waals-kræfter). Efterhånden som molekylerne får energi, vibrerer de kraftigere, overvinder disse kræfter og bryder fri fra væskens overflade.
3. Ændring af stat: Når molekylerne har energi nok, undslipper de væskens overflade og går ind i gasform.
To hovedtyper af fordampning:
* Fordampning: Dette er en gradvis proces, der forekommer ved overfladen af en væske ved enhver temperatur. Molekyler med højere kinetisk energi undslipper væsken og bliver til damp. Det er derfor vandpytter til sidst tørrer op, selv på kølige dage.
* Kogning: Dette sker, når væsken når sit kogepunkt, den temperatur, ved hvilken væskens damptryk er lig med trykket omkring den. Væsken ændres derefter til en gas gennem hele volumen, ikke kun ved overfladen.
Faktorer, der påvirker fordampning:
* Temperatur: Højere temperaturer fører til hurtigere fordampning.
* Overfladeareal: Større overfladearealer tillader flere molekyler at undslippe ind i gasfasen.
* Atmosfærisk tryk: Lavere atmosfærisk tryk gør det lettere for molekyler at undslippe ind i gasfasen.
Opsummeret bliver væske til gas, når molekylerne får nok energi til at overvinde de kræfter, der holder dem sammen i flydende tilstand. Denne proces kaldes fordampning, og den kan forekomme gradvist (fordampning) eller hurtigt (kogning).
 Varme artikler
Varme artikler
-
 Polymermembraner kunne have fordel af at tage en dukkertI forsøget, forskere dykkede først en hydrofob polymer membran i garvesyre (TA), en almindelig polyfenol. Derefter, den tørrede TA dip-coatede membran fyldes i atomlagsaflejringsreaktoren (ALD) til ov
Polymermembraner kunne have fordel af at tage en dukkertI forsøget, forskere dykkede først en hydrofob polymer membran i garvesyre (TA), en almindelig polyfenol. Derefter, den tørrede TA dip-coatede membran fyldes i atomlagsaflejringsreaktoren (ALD) til ov -
 Hvorfor træ fyrer af pop og knitren:Videnskaben bag lydenAf Chris Deziel | Opdateret 30. august 2022 HannahDewey/iStock/Getty Images TL;DR Den knitren og knalden, du hører fra en brændebrand, er forårsaget af hurtig udvidelse og frigivelse af forbrændings
Hvorfor træ fyrer af pop og knitren:Videnskaben bag lydenAf Chris Deziel | Opdateret 30. august 2022 HannahDewey/iStock/Getty Images TL;DR Den knitren og knalden, du hører fra en brændebrand, er forårsaget af hurtig udvidelse og frigivelse af forbrændings -
 Vil dit fremtidige tøj være lavet af alger?En mini-T-shirt demonstrerer de fotosyntetiske levende materialer skabt i laboratoriet af University Rochester biolog Anne S. Meyer og Delft University of Technology bionanoforsker Marie-Eve Aubin-Tam
Vil dit fremtidige tøj være lavet af alger?En mini-T-shirt demonstrerer de fotosyntetiske levende materialer skabt i laboratoriet af University Rochester biolog Anne S. Meyer og Delft University of Technology bionanoforsker Marie-Eve Aubin-Tam -
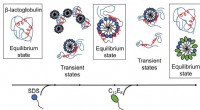 Fanget i sæbehånd:At forstå, hvordan sæbemolekyler hjælper proteiner med at komme ind og ud af …Resultater offentliggjort af AU-forskere afslører, at surfaktant-medieret udfoldning og genfoldning af proteiner er komplekse processer med flere strukturer til stede, og omarrangeringer sker på tidss
Fanget i sæbehånd:At forstå, hvordan sæbemolekyler hjælper proteiner med at komme ind og ud af …Resultater offentliggjort af AU-forskere afslører, at surfaktant-medieret udfoldning og genfoldning af proteiner er komplekse processer med flere strukturer til stede, og omarrangeringer sker på tidss


