Elektrontælling i Lewis-strukturer:Forståelse af oktetter og binding
Her er opdelingen:
* Oktetregel: Oktetreglen siger, at atomer har tendens til at vinde, miste eller dele elektroner for at opnå en stabil konfiguration med otte elektroner i deres yderste skal (valensskal).
* Lewis-strukturer: Det er diagrammer, der viser bindingen mellem atomer og de enlige elektronpar, der kan eksistere i et molekyle.
* Tælle elektroner: Antallet af elektroner involveret i en Lewis-struktur afhænger af de specifikke involverede atomer og de bindinger, de danner.
Eksempel:
* Vand (H₂O): Ilt har 6 valenselektroner, og hver brint har 1. For at opnå en oktet har oxygen brug for 2 elektroner mere, som den får ved at danne to enkeltbindinger med brintatomerne. Der er i alt 8 elektroner i Lewis-strukturen af vand (2 fra hver brint og 4 fra oxygen).
Sammenfattende er der ingen "oktetter af elektroner" i en Lewis-struktur. I stedet tæller du det samlede antal valenselektroner, der deltager i bindings- og ensommeparret.
 Varme artikler
Varme artikler
-
 Forskere ser kemisk rækkevidde i mellem-entropi-legeringKredit:CC0 Public Domain Kinesiske forskere har foretaget direkte observationer af ansigtscentrerede kubiske VCoNi (medium) -entropylegeringer (MEA) og for første gang foreslået en overbevisende i
Forskere ser kemisk rækkevidde i mellem-entropi-legeringKredit:CC0 Public Domain Kinesiske forskere har foretaget direkte observationer af ansigtscentrerede kubiske VCoNi (medium) -entropylegeringer (MEA) og for første gang foreslået en overbevisende i -
 Aerogel integreret træ giver bedre isolering end eksisterende plastbaserede materialerEt nærbillede af aerogelen til isolering, udviklet af træcellulose. Kredit:Jonas Garemark/Wallenberg Wood Science Center, KTH Royal Institute of Technology En dag snart kan bygninger blive mere ene
Aerogel integreret træ giver bedre isolering end eksisterende plastbaserede materialerEt nærbillede af aerogelen til isolering, udviklet af træcellulose. Kredit:Jonas Garemark/Wallenberg Wood Science Center, KTH Royal Institute of Technology En dag snart kan bygninger blive mere ene -
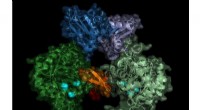 Forskerhold finder mulig ny tilgang til sovesygemedicinStruktur af parasittens IMP-dehydrogenase. Det aktive enzym danner par (dimerer), switch-området (Bateman-regionen) vises i blå nuancer. Kredit:Lübeck Universitet/DESY, Lars Redecke Ved hjælp af u
Forskerhold finder mulig ny tilgang til sovesygemedicinStruktur af parasittens IMP-dehydrogenase. Det aktive enzym danner par (dimerer), switch-området (Bateman-regionen) vises i blå nuancer. Kredit:Lübeck Universitet/DESY, Lars Redecke Ved hjælp af u -
 Forskning går til nye dybder i hudpeptidundersøgelserDavid Scurr, Seniorforsker, Farmaceutisk Skole. Kredit:University of Nottingham Forskere har for første gang afsløret, at et peptid i et førende skønhedsprodukt kan trænge ind i hudens hårde strat
Forskning går til nye dybder i hudpeptidundersøgelserDavid Scurr, Seniorforsker, Farmaceutisk Skole. Kredit:University of Nottingham Forskere har for første gang afsløret, at et peptid i et førende skønhedsprodukt kan trænge ind i hudens hårde strat
- Varmebehandling kan gøre kemoterapi mere effektiv
- Hvad er nogle spørgsmål, som videnskaben besvarer?
- Bugbid fra strandsand
- Coronavirus har ændret vores følelse af sted, så sammen må vi genskabe vores byer
- Den type klipper, der dannes, hvor de rester planter og dyr afsættes i tykke lag, der kaldes?
- COVID-19-vacciner har affødt ni nye milliardærer:kampagnegruppe


