Forståelse af faseændringer:fast, flydende, gas og overgange
Her er en opdeling:
* Særlige forhold: Stof findes i forskellige tilstande, de mest almindelige er fast, flydende og gas. Hver stat har forskellige egenskaber:
* Solid: Fast form og volumen.
* Væske: Fast volumen, men tager form af sin beholder.
* Gas: Ingen fast form eller volumen, udvides for at fylde sin beholder.
* Faseændringer: Overgangene mellem disse tilstande kaldes faseændringer:
* Smeltning: Fast til flydende (f.eks. is til vand).
* Fryser: Væske til fast (f.eks. vand til is).
* Fordampning: Væske til gas (f.eks. vand til damp).
* Kondensering: Gas til væske (f.eks. damp til vand).
* Sublimering: Fast til gas (f.eks. tøris til kuldioxidgas).
* Deponering: Gas til fast stof (f.eks. vanddamp til frost).
Hvad driver faseændringer?
Faseændringer opstår på grund af ændringer i temperatur og tryk . Når energi tilføres (som varme), bevæger molekyler sig hurtigere og overvinder intermolekylære kræfter, hvilket forårsager overgange til mindre tætte tilstande (f.eks. smeltning, fordampning). Når energi fjernes, sænker molekylerne farten, hvilket fører til overgange til tættere tilstande (f.eks. frysning, kondensation).
Eksempler:
* Kogende vand: Tilførsel af varme får flydende vandmolekyler til at få nok energi til at undslippe som damp.
* Issmeltning: Tilførsel af varme får vandmolekylerne i is til at bryde deres stive struktur og bevæge sig mere frit som flydende vand.
* Dugdannelse: Kølende luft får vanddamp i luften til at kondensere til små vanddråber på overflader.
Sig til, hvis du vil have mere information om en specifik faseændring!
 Varme artikler
Varme artikler
-
 Forståelse af butanbrændstof:egenskaber, anvendelser og sikkerhedHvad er butan? Butan er en brændbar, farveløs gas, der forbliver flydende under moderat tryk. Det er en primær komponent i mange husholdningsbrændstoffer, især cigarettændere og bærbare madlavningsap
Forståelse af butanbrændstof:egenskaber, anvendelser og sikkerhedHvad er butan? Butan er en brændbar, farveløs gas, der forbliver flydende under moderat tryk. Det er en primær komponent i mange husholdningsbrændstoffer, især cigarettændere og bærbare madlavningsap -
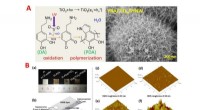 Nyt foreslået strategi tilbyder smart fleksibel neural elektrode med høj effektivitetA. (a) Skematisk diagram af accelereret PDA-polymerisation med nano-TiO 2 og UV, (b) SEM for PDA/TiO 2 /PtNW modificeret elektrode. B. (a) Prøver af forskellige coatede elektroder (1 cm × 1 cm). (
Nyt foreslået strategi tilbyder smart fleksibel neural elektrode med høj effektivitetA. (a) Skematisk diagram af accelereret PDA-polymerisation med nano-TiO 2 og UV, (b) SEM for PDA/TiO 2 /PtNW modificeret elektrode. B. (a) Prøver af forskellige coatede elektroder (1 cm × 1 cm). ( -
 Bakterieappetit kan være nøglen til at rydde op i antibiotikaforureningAntibiotika i miljøet bidrager til lægemiddelresistens. Men forskere ved Washington University School of Medicine i St. Louis har fundet ud af, hvordan nogle jordbakterier forvandler stofferne til mad
Bakterieappetit kan være nøglen til at rydde op i antibiotikaforureningAntibiotika i miljøet bidrager til lægemiddelresistens. Men forskere ved Washington University School of Medicine i St. Louis har fundet ud af, hvordan nogle jordbakterier forvandler stofferne til mad -
 Forbedring af genleveringsmetoderKredit:Royal Society of Chemistry Forskere i Kina undersøger nye måder at behandle kræft på ved hjælp af genterapi. Vi finder ud af, hvordan deres arbejde inspirerede dette smukke og indviklede de
Forbedring af genleveringsmetoderKredit:Royal Society of Chemistry Forskere i Kina undersøger nye måder at behandle kræft på ved hjælp af genterapi. Vi finder ud af, hvordan deres arbejde inspirerede dette smukke og indviklede de
- Copolymer hjælper med at fjerne gennemtrængende PFAS-toksiner fra miljøet
- Ændringer i marine økosystemer bliver uopdaget
- Pandemi affaldsboom sætter gang i debat om affald som energi
- Hvad er et eksempel på homogen blanding?
- Hvad er minedrift ved fjernelse af bjergtop?
- Hvad er synonymer for kinetisk energi?


