Ammoniumchlorid- og sølvnitratreaktion:afbalanceret ligning og forklaring
NH₄Cl(aq) + AgNO₃(aq) → AgCl(s) + NH₄NO3(aq)
Her er en oversigt over reaktionen:
* Reaktanter:
* Ammoniumchlorid (NH4Cl) er en farveløs ionisk forbindelse.
* Sølvnitrat (AgNO₃) er også en farveløs ionforbindelse.
* Produkter:
* Sølvchlorid (AgCl) er et hvidt, uopløseligt fast stof, der udfældes fra opløsningen.
* Ammoniumnitrat (NH₄NO₃) er en farveløs ionforbindelse, der forbliver opløst i opløsningen.
Forklaring:
Denne reaktion er en dobbelt forskydningsreaktion, hvilket betyder, at de positive og negative ioner skifter partner. Sølvionerne (Ag⁺) fra sølvnitrat reagerer med chloridionerne (Cl⁻) fra ammoniumchlorid og danner sølvchlorid (AgCl), som er uopløseligt i vand og danner et hvidt bundfald. Ammoniumionerne (NH4+) og nitrationerne (NO3⁻) forbliver i opløsning som ammoniumnitrat (NH4NO3).
Nøglepunkter:
* Reaktionen er afbalanceret, hvilket betyder, at der er lige mange af hver type atom på begge sider af ligningen.
* Tilstandssymbolerne angiver den fysiske tilstand af hvert stof:(aq) for vandig (opløst i vand) og (s) for fast stof.
* Denne reaktion kan bruges til at teste for tilstedeværelsen af chloridioner i en opløsning.
 Varme artikler
Varme artikler
-
 Ny måde at opdage ekstase påKredit:Syddansk Universitet Mens man bygger molekylære maskiner, forskere faldt over en ny metode til at opdage ekstase. Opdagelsen kan føre til mere pålidelige lægemiddeltest. Forskere ved Sydda
Ny måde at opdage ekstase påKredit:Syddansk Universitet Mens man bygger molekylære maskiner, forskere faldt over en ny metode til at opdage ekstase. Opdagelsen kan føre til mere pålidelige lægemiddeltest. Forskere ved Sydda -
 Låser op for effektiv lys-energikonvertering med stabile koordinationsnanoarkKredit:Hiroshi Nishihara fra Tokyo University of Science To-dimensionelle nanosheets lavet af bindinger mellem metalatomer og organiske molekyler er attraktive kandidater til fotoelektrisk omdanne
Låser op for effektiv lys-energikonvertering med stabile koordinationsnanoarkKredit:Hiroshi Nishihara fra Tokyo University of Science To-dimensionelle nanosheets lavet af bindinger mellem metalatomer og organiske molekyler er attraktive kandidater til fotoelektrisk omdanne -
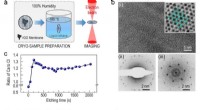 Nyligt observeret monovalent calciumion viser uventet metallicitet og ferromagnetisme(a) Skematiske tegninger af prøveforberedelsesprocesserne. (b) (i) Cryo-EM billede af Ca-Cl krystallerne i den ultratynde reducerede grafenoxid (rGO) membran. (ii) diffraktionsmønster for en typisk kr
Nyligt observeret monovalent calciumion viser uventet metallicitet og ferromagnetisme(a) Skematiske tegninger af prøveforberedelsesprocesserne. (b) (i) Cryo-EM billede af Ca-Cl krystallerne i den ultratynde reducerede grafenoxid (rGO) membran. (ii) diffraktionsmønster for en typisk kr -
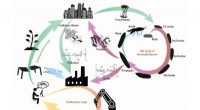 Team udvikler manglende led til cirkulær økonomi, mens de tackler globalt affaldSkematisk over det udviklede lukkede produktionskredsløb baseret på bioinspirerede kitinholdige materialer og biokonvertering i et bymiljø. Kredit:SUTD Forskere fra Singapore University of Technol
Team udvikler manglende led til cirkulær økonomi, mens de tackler globalt affaldSkematisk over det udviklede lukkede produktionskredsløb baseret på bioinspirerede kitinholdige materialer og biokonvertering i et bymiljø. Kredit:SUTD Forskere fra Singapore University of Technol
- Hvor mange orbitaler er der i andet energiniveau?
- Nanooscillatorer synkroniseret med lys
- Fotosyntese:Dannelse af C-C-bindinger i kulhydrater
- Simulering viser, at det er muligt at flytte H2O@C60 ved hjælp af elektrisk ladning
- Hvad er symbiotiske forhold?
- Et kig ind i Amazons nye Minnesota-facilitet:Bederum, afvaskningsstationer og slisker og stiger


