Hydrogenbinding i Ortho- og Para-Nitrophenol:En detaljeret forklaring
Krav til hydrogenbinding:
* Brintbindingsdonor: Et hydrogenatom, der er kovalent bundet til et meget elektronegativt atom (som oxygen eller nitrogen).
* Brintbindingsacceptor: Et elektronegativt atom med et ensomt elektronpar.
I ortho-nitrophenol og para-nitrophenol:
* Brintbindingsdonor: Hydrogenatomet bundet til oxygenet i hydroxylgruppen (-OH).
* Brintbindingsacceptor: Oxygenatomet i nitro (-NO2) gruppen.
Ortho-nitrophenol:
* På grund af den tætte nærhed af hydroxyl- og nitrogrupperne dannes der en stærk intramolekylær hydrogenbinding mellem hydroxylgruppens hydrogen og nitrogruppens oxygen. Denne intramolekylære hydrogenbinding påvirker i væsentlig grad egenskaberne af ortho-nitrophenol, hvilket gør det mere flygtigt og mindre surt end para-nitrophenol.
Para-nitrophenol:
* Hydroxyl- og nitrogrupperne er længere fra hinanden i para-nitrophenol, hvilket forhindrer intramolekylær hydrogenbinding. Para-nitrophenol kan dog stadig deltage i intermolekylær hydrogenbinding med andre para-nitrophenol-molekyler eller med opløsningsmiddelmolekyler.
Opsummering:
* Ortho-nitrophenol har både intramolekylær og intermolekylær hydrogenbinding.
* Para-nitrophenol har kun intermolekylær hydrogenbinding.
Tilstedeværelsen af hydrogenbinding påvirker forskellige egenskaber af disse forbindelser, herunder smeltepunkt, kogepunkt, opløselighed og surhed.
 Varme artikler
Varme artikler
-
 Træ du kan lide en drink? Japans hold opfinder træspritRåmateriale? Japanske forskere siger, at de har opfundet en måde at producere alkoholholdige drikkevarer fra kirsebærtræer og andre træsorter Kræsne drikkere kan snart blive forgrenet, efter at ja
Træ du kan lide en drink? Japans hold opfinder træspritRåmateriale? Japanske forskere siger, at de har opfundet en måde at producere alkoholholdige drikkevarer fra kirsebærtræer og andre træsorter Kræsne drikkere kan snart blive forgrenet, efter at ja -
 Blomsterlignende nanostrukturer i natriumbatterierNatrium-ion-batterier (SIB) er varme kandidater til en billig og bæredygtig batteriteknologi, men et tilbagevendende problem er anode-ustabilitet. Et kinesisk hold af videnskabsmænd rapporterer nu om
Blomsterlignende nanostrukturer i natriumbatterierNatrium-ion-batterier (SIB) er varme kandidater til en billig og bæredygtig batteriteknologi, men et tilbagevendende problem er anode-ustabilitet. Et kinesisk hold af videnskabsmænd rapporterer nu om -
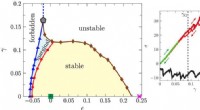 Er amorfe faste stoffer elastiske eller plastiske?Til venstre:Stabilitets-reversibilitetskort over amorfe faste stoffer i hårde kugler, repræsenteret med hensyn til volumen og forskydningsbelastninger. Til højre:Typiske stress-strain-kurver, som vise
Er amorfe faste stoffer elastiske eller plastiske?Til venstre:Stabilitets-reversibilitetskort over amorfe faste stoffer i hårde kugler, repræsenteret med hensyn til volumen og forskydningsbelastninger. Til højre:Typiske stress-strain-kurver, som vise -
 En nyopdaget katalysator lover billigere brintproduktionKredit:American Chemical Society En ny katalysator kan dramatisk reducere omkostningerne ved at producere brint, et af de reneste vedvarende brændstoffer. Baseret på molybdensulfid, katalysatoren
En nyopdaget katalysator lover billigere brintproduktionKredit:American Chemical Society En ny katalysator kan dramatisk reducere omkostningerne ved at producere brint, et af de reneste vedvarende brændstoffer. Baseret på molybdensulfid, katalysatoren
- En ultrafortyndet kvantevæske lavet af ultrakolde atomer
- Sex tech har til formål at hæve sig over det negative image
- Er gammel rock virkelig lige så 'solid a rock'?
- Er sulfat en fast eller vandig opløsning?
- Forskerhold opdager en ny måde at lave en næsten perfekt lysabsorber
- Hvad er en neogen rekombinator?


