Hvorfor kovalente forbindelser ikke leder elektricitet (selv smeltet)
* Kovalente bindinger: I kovalente bindinger deles elektroner mellem atomer. Disse delte elektroner holdes tæt inde i molekylet og er ikke frie til at bevæge sig rundt.
* Smeltning: Smeltning af en kovalent forbindelse svækker de intermolekylære kræfter, hvilket tillader molekylerne at bevæge sig mere frit. Imidlertid forbliver elektronerne i molekylerne bundet og er ikke i stand til at bære en elektrisk strøm.
Kontrast med ioniske forbindelser:
Ioniske forbindelser er på den anden side gode ledere af elektricitet, når de smeltes. Dette er fordi:
* Ionbindinger: I ionbindinger overføres elektroner fra et atom til et andet, hvilket skaber positive og negative ioner.
* Smeltning: Når en ionforbindelse smelter, bliver ionerne frie til at bevæge sig, så de kan bære en elektrisk strøm.
Eksempler:
* Dårlige ledere (kovalente): Sukker (saccharose), vand (H₂O), metan (CH₄)
* Gode ledere (ioniske): Natriumchlorid (NaCl), kaliumbromid (KBr), calciumoxid (CaO)
 Varme artikler
Varme artikler
-
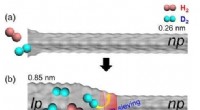 Ny strategi for isotopadskillelse med fleksibelt porøst materialevejrtrækning af MIL-53(Al), en fleksibel metal-organisk ramme (MOF). Kredit:UNIST En ny undersøgelse foretaget af et internationalt hold af forskere tilknyttet UNIST er lykkedes med at udvikle en
Ny strategi for isotopadskillelse med fleksibelt porøst materialevejrtrækning af MIL-53(Al), en fleksibel metal-organisk ramme (MOF). Kredit:UNIST En ny undersøgelse foretaget af et internationalt hold af forskere tilknyttet UNIST er lykkedes med at udvikle en -
 Forskere udvikler banebrydende røntgenteknik til at analysere gamle artefakterFotografier af arkæologiprøverne. Kredit:University of Leicester En banebrydende røntgenteknik, der kan analysere artefakter af enhver form eller tekstur på en ikke-destruktiv måde, er blevet udvi
Forskere udvikler banebrydende røntgenteknik til at analysere gamle artefakterFotografier af arkæologiprøverne. Kredit:University of Leicester En banebrydende røntgenteknik, der kan analysere artefakter af enhver form eller tekstur på en ikke-destruktiv måde, er blevet udvi -
 En metode til computerstøttet modellering og simulering af store proteiner og andre biomolekylerKredit:CC0 Public Domain To computerforskere ved Freie Universität Berlin ændrer måden, store proteiner modelleres inde i computere ved at kombinere maskinlæring, et område med kunstig intelligens
En metode til computerstøttet modellering og simulering af store proteiner og andre biomolekylerKredit:CC0 Public Domain To computerforskere ved Freie Universität Berlin ændrer måden, store proteiner modelleres inde i computere ved at kombinere maskinlæring, et område med kunstig intelligens -
 Hvad din stemningsringfarve virkelig siger om dine følelserD_Lux/Shutterstock Da stemningsringe debuterede i 1975, udløste de et kulturelt fænomen, der fangede offentlighedens fantasi. Inden for tre måneder solgte detailhandlere 40 millioner ringe sammen me
Hvad din stemningsringfarve virkelig siger om dine følelserD_Lux/Shutterstock Da stemningsringe debuterede i 1975, udløste de et kulturelt fænomen, der fangede offentlighedens fantasi. Inden for tre måneder solgte detailhandlere 40 millioner ringe sammen me
- Hvilke forfininger måtte foretages i atomteori, der tegner sig for resultater på de kombinerende m…
- Hvilken videnskabsmand ville studere udvikling af sprog?
- Hvilke to former for energi er vi mest kendte?
- Hvorfor ser Moon til os oplyst?
- Hvordan sparer du atomenergi?
- Hvad er den samlede mængde kinetisk energi og potentiale i et system?


