Metallisk binding vs. kovalent binding:Hvorfor metaller ikke danner gigantiske kovalente strukturer
* Metallisk binding: Metaller danner metalliske bindinger, ikke kovalente bindinger. Metallisk binding involverer et "hav" af delokaliserede elektroner, der deles af alle metalatomerne i strukturen. Disse elektroner kan frit bevæge sig gennem metallet, hvilket giver metaller deres fremragende ledningsevne.
* Kovalent binding: Kovalent binding involverer deling af elektroner mellem atomer for at danne stærke bindinger. Disse elektroner er lokaliseret mellem atomerne og kan ikke bevæge sig frit.
Her er en opdeling af egenskaberne af metaller og gigantiske kovalente strukturer:
| Ejendom | Metaller | Kæmpe kovalente strukturer |
|---|---|---|
| Limningstype | Metallisk | Kovalent |
| Elektrisk ledningsevne | Fremragende | Dårlig (undtagen grafit) |
| Formbarhed | Høj | Generelt sprøde |
| Duktilitet | Høj | Generelt sprøde |
| Smeltepunkt | Generelt høj | Generelt høj (undtagen grafit) |
Eksempler:
* Metaller: Jern, kobber, guld, natrium
* Kæmpe kovalente strukturer: Diamant, siliciumdioxid (kvarts)
Opsummering: Metaller er fremragende ledere af elektricitet på grund af deres metalliske binding, som giver mulighed for fri bevægelse af elektroner. Kæmpe kovalente strukturer har på den anden side lokaliserede elektroner og er generelt dårlige ledere.
 Varme artikler
Varme artikler
-
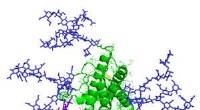 Kroppen er afhængig af tusinder af sukker -proteinkomplekser for at forblive sundEn model af erythropoetin, et glycoprotein involveret i produktionen af røde blodlegemer. Glykaner er angivet med lilla. Kredit:Mark Wormald, Oxford Glycobiology Institute Over to uger i 2004, S
Kroppen er afhængig af tusinder af sukker -proteinkomplekser for at forblive sundEn model af erythropoetin, et glycoprotein involveret i produktionen af røde blodlegemer. Glykaner er angivet med lilla. Kredit:Mark Wormald, Oxford Glycobiology Institute Over to uger i 2004, S -
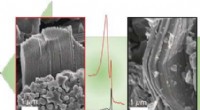 Titaniumcarbidflager opnået ved selektiv ætsning af titaniumsiliciumcarbidKredit:Wiley Metallisk ledningsevne og hydrofilicitet af MXenes har etableret dem som elektroder i genopladelige batterier og superkondensatorer, såvel som andre applikationer, herunder fototermis
Titaniumcarbidflager opnået ved selektiv ætsning af titaniumsiliciumcarbidKredit:Wiley Metallisk ledningsevne og hydrofilicitet af MXenes har etableret dem som elektroder i genopladelige batterier og superkondensatorer, såvel som andre applikationer, herunder fototermis -
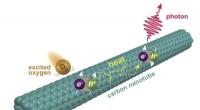 Kemikere får et kig på ny fluorescens i kulstofnanorørKemikere ved Rice University har opdaget et andet niveau af fluorescens i enkeltvæggede kulstofnanorør. Fluorescensen udløses, når oxygenmolekyler exciteret til en singlettilstand interagerer med nano
Kemikere får et kig på ny fluorescens i kulstofnanorørKemikere ved Rice University har opdaget et andet niveau af fluorescens i enkeltvæggede kulstofnanorør. Fluorescensen udløses, når oxygenmolekyler exciteret til en singlettilstand interagerer med nano -
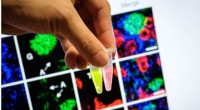 Forskere udvikler sonder til at opdage akut nyresvigt tidligtSonderne, når det tilsættes en urinprøve med biomarkører, der indikerer begyndelsen af akut nyresvigt, lyser, når de udsættes for UV-lys. De gør det 36 timer hurtigere end andre molekylære billeddan
Forskere udvikler sonder til at opdage akut nyresvigt tidligtSonderne, når det tilsættes en urinprøve med biomarkører, der indikerer begyndelsen af akut nyresvigt, lyser, når de udsættes for UV-lys. De gør det 36 timer hurtigere end andre molekylære billeddan
- Hvilken del kontrollerer aktiviteten af en cell?
- Hvor genetisk teknik bruges i landbruget?
- Forskere udvikler et nanohybrid -køretøj til optimalt at levere medicin til menneskekroppen
- Opsamling og lagring af kulstof i jord:Er det ægte dåseskalering?
- Hvad henviser potentiel energi til?
- Hvorfor betragtes blade som stof?


